在 K2Cr2O7+8HCl═2KCl+2CrCl3+3Cl2+4H2O反应中.(1)______元
| 在 K2Cr2O7+8HCl═2KCl+2CrCl3+3Cl2+4H2O反应中. (1)______元素被氧化,______是氧化剂. (2)______是氧化产物,______发生氧化反应. (3)在参加反应的盐酸中,起还原剂(被氧化)作用的HCl与起酸性作用的HCl的质量比为______. (4)用线桥法标明电子转移的方向和数目.______. |
参考解答
| (1)化合价升高的元素是氯元素,被氧化,K2Cr2O7中铬元素的化合价降低,为氧化剂,故答案为:氯;K2Cr2O7; (2)化合价升高的氯元素所在的生成物氯气是氧化产物,HCl做还原剂被氧化,发生氧化反应,故答案为:Cl2、HCl; (3)起还原剂(被氧化)作用的HCl为6mol,起酸性作用的HCl为8mol,物质的量之比=质量比=3:4,故答案为:3:4; (4)氧化还原反应的电子转移情况是: 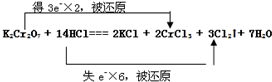 ,故答案为:  . |
相似问题
人体正常的血红蛋白中含有Fe2+ 若误食亚硝酸盐 则使血红蛋白中Fe2+转化为Fe3+丧失其生理功能
人体正常的血红蛋白中含有Fe2+,若误食亚硝酸盐,则使血红蛋白中Fe2+转化为Fe3+丧失其生理功能,临床证明服用维生素C可以解毒.下列叙述正确的是( )
下列反应中 通入的气体物质只作为氧化剂的是( )A.NO2通入水中B.Cl2通入FeCl2溶液中C
下列反应中,通入的气体物质只作为氧化剂的是( )A.NO2通入水中B.Cl2通入FeCl2溶液中C.SO2通入NaOH溶液中D.Cl2通入KOH溶液中
氧化还原反应的实质是( )A.氧元素的得与失B.化合价的升降C.电子的得失或偏移D.分子中原子重新
氧化还原反应的实质是( )A.氧元素的得与失B.化合价的升降C.电子的得失或偏移D.分子中原子重新组合
2007年10月 一台湾女孩因食用河虾后服用大剂量的维生素C而中毒.菜谱中记载:河虾不宜与西红柿同食
2007年10月,一台湾女孩因食用河虾后服用大剂量的维生素C而中毒.菜谱中记载:河虾不宜与西红柿同食.主要原因是河虾中含有五价砷,西红柿中含有比较多的
下列叙述中正确的是( )A.纯碱从物质的分类看不属于碱B.化合反应都属于氧化还原反应C.单质只能用
下列叙述中正确的是( )A.纯碱从物质的分类看不属于碱B.化合反应都属于氧化还原反应C.单质只能用置换反应制取D.含氧元素的化合物称为氧化物












