储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒 这种碳纳米
| 储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化汽化法提纯。其反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3、H2O七种物质。 (1)请用上述物质填空,并配平化学方程式: 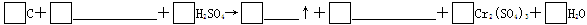 (2)上述反应中氧化剂是(填化学式)_______________,被氧化的元素是(填元素符号)_____________。 (3)H2SO4在上述反应中表现出来的性质是(填选项编号)____________________。 A.氧化性 B.酸性 C.氧化性和酸性 D.还原性和酸性 (4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为________升。 |
参考解答
| (1)3 2K2Cr2O7 8 3CO2 2K2SO4 2 8 (共2分,其中配平1分,化学式1分) (2)K2Cr2O7 C (各2分) (3)B (1分) (4)4.48 (2分) |
试题分析:(1)由C→CO2、K2Cr2O7→Cr2(SO4)3可知,碳元素的化合价从0价升高到+4价,失去4个电子。Cr元素的化合价从+6价降低到+3价,得到3个电子,所以根据电子得失守恒可知还原剂与氧化剂的物质的量之比是3:2。根据原子守恒可知,反应中还有硫酸钾生成,则反应的化学方程式为3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。 (2)根据(1)可知氧化剂为K2Cr2O7,还原产物为Cr2(SO4)3,还原剂为C,氧化产物为CO2,被氧化的元素是C。 (3)H2SO4在反应中各元素的化合价没有发生变化,但反应中有硫酸盐生成,所以硫酸只表现酸性,答案选B。 (4)设产生的气体的体积为V,根据反应式计算: 3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O转移电子 33.6L 12mol V 0.8mol 解得V= 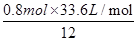 =4.48L =4.48L |
相似问题
(8分)实验室里迅速制备少量氯气可利用以下反应:2 KMnO4+16 HCl ='==' 2 KCl
(8分)实验室里迅速制备少量氯气可利用以下反应:2 KMnO4+16 HCl ="==" 2 KCl + 2 MnCl2 + 5 Cl2↑ + 8 H2O 此反应不需要加热,常温下就可
通过对模型 图形 图表的观察 能获取有关信息是化学学习的一种重要能力。按要求回答下列问题。(1) 现
通过对模型、图形、图表的观察,能获取有关信息是化学学习的一种重要能力。按要求回答下列问题。(1) 现有下列短周期元素性质的部分数据,其中X数值是表
已知2Fe2++Br2=2Fe3++2Br-。向100mL的FeBr2溶液中通入标准状况下的Cl2
已知2Fe2++Br2=2Fe3++2Br-。向100mL的FeBr2溶液中通入标准状况下的Cl2 3 36L,充分反应后测得溶液中Cl-与Br-的物质的量浓度相等,则原FeBr2溶液的
(1)(8分)某反应体系中的物质有NaOH Au2O3 Na2S4O6 Au2O H2O Na2S2
(1)(8分)某反应体系中的物质有NaOH、Au2O3,Na2S4O6,Au2O,H2O,Na2S2O3。Au2O3为反应物,回答下列部题A.NaOH是(反应物、生成物)B.Na2S4O6是(
(1小题1分 2 3小题各2分 共5分)用15.8g KMnO4与12mol/L的浓HCl发生。反应
(1小题1分,2、3小题各2分,共5分)用15 8g KMnO4与12mol L的浓HCl发生。反应方程式如下:2KMnO4+ 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑+ 8H












