高铁酸钾(K2FeO4)是一种集氧化 吸附 絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:请同
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下: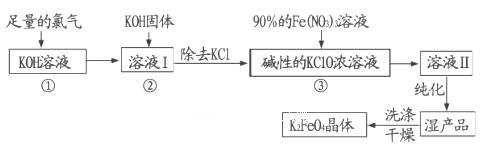 请同答下列问题: (l)写出向KOH溶液中通入足量Cl2发生反应的离子方程式_______ 。 (2)在溶液I中加入KOH固体的目的是______(填编号)。
(4)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:_______ FeO42-+_______ H2O="_______" Fe(OH)3(胶体)+_______O2↑+_______OH-。 (5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图所示。电解过程中阳极的电极反应式为________。 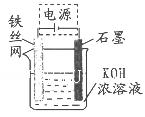 (6)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:3Zn(OH)2+2Fe(OH)3+4KOH-----3Zn+2K2FeO4+8H2O,放电时电池的负极反应式为________ 。 |
参考解答
| (1)2OH-+Cl2=ClO-+Cl-+H2O (2) AC (3) 2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O 0.45 (4) 4FeO42- +10H2O  4Fe(OH)3 (胶体) +3O2↑+8 OH- (5) Fe+8OH—6e-= FeO42- -+4H2O 4Fe(OH)3 (胶体) +3O2↑+8 OH- (5) Fe+8OH—6e-= FeO42- -+4H2O(6)Zn+2OH—2e-=Zn(OH)2或Zn+2OH=Zn(OH)2+2e-。 |
试题分析:(l) KOH溶液与足量Cl2发生反应的离子方程式为2OH-+Cl2=ClO-+Cl-+H2O。(2)在溶液I中加入KOH固体的目的是为下一步反应提供碱性的环境;与溶液I中过量的Cl2继续反应,生成更多的KClO。故选项为A. C.(3) 反应③中发生的离子反应方程式为2Fe3++3ClO-+10OH-=2FeO42-+ Cl-+5H2O .在方程式中每产生2mol的FeO42-转移电子6mol.消耗氧化剂3mol.现在n(K2FeO4)= 59.4g÷198g/mol=0.3mol所以消耗氧化剂的物质的量为3÷2×0.3mol=0.45mol.(4) 高铁酸钾(K2FeO4)水解的离子方程式为4FeO42- +10H2O  4Fe(OH)3 (胶体) +3O2↑+8 OH-(5) 电解法是制备K2FeO4较好的方法,Fe作阳极,电极反应为Fe+8OH—6e-= FeO42- +4H2O,石墨作阴极,电极反应为:O2+ 2H2O+4e-=4OH—.(6)高铁电池放电时电池的负极反应式为Zn+2OH—2e-=Zn(OH)2。2FeO4)的制法、原理、电子转移及高铁电池等反应原理的知识。 4Fe(OH)3 (胶体) +3O2↑+8 OH-(5) 电解法是制备K2FeO4较好的方法,Fe作阳极,电极反应为Fe+8OH—6e-= FeO42- +4H2O,石墨作阴极,电极反应为:O2+ 2H2O+4e-=4OH—.(6)高铁电池放电时电池的负极反应式为Zn+2OH—2e-=Zn(OH)2。2FeO4)的制法、原理、电子转移及高铁电池等反应原理的知识。 |
相似问题
氮气及含氮的化合物在国民经济中占有重要地位。合成氨工业中 合成塔中每产生2 mol NH3 放出92
氮气及含氮的化合物在国民经济中占有重要地位。合成氨工业中,合成塔中每产生2 mol NH3,放出92 4 kJ热量。 (1)若起始时向容器内放入2 mol N2和6
若(NH4)2SO4在强热时分解的产物是SO2 N2 NH3和H2O 则该反应中化合价发生变化和未发
若(NH4)2SO4在强热时分解的产物是SO2、N2、NH3和H2O,则该反应中化合价发生变化和未发生变化的N原子数之比为( )A.1:4B.1:2C.2:1D.4:1
把一定质量的铁完全溶解于某浓度的硝酸中收集到0.3 mol NO2和0.2 mol NO。向反应后的
把一定质量的铁完全溶解于某浓度的硝酸中收集到0 3 mol NO2和0 2 mol NO。向反应后的溶液中加入足量NaOH溶液充分反应,经过滤、洗涤后,把所得沉淀加
有一铁的氧化物样品 用140 mL 5 mol·L-1盐酸可恰好使其完全溶解。所得溶液可吸收标准状况
有一铁的氧化物样品,用140 mL 5 mol·L-1盐酸可恰好使其完全溶解。所得溶液可吸收标准状况下0.56 L氯气,使其中的Fe2+全部转化为Fe3+。该样品可
下列叙述不正确的是A.Li+中含有的中子数与电子数之比为2︰1B.在C2H6分子中极性共价键与非极性
下列叙述不正确的是A.Li+中含有的中子数与电子数之比为2︰1B.在C2H6分子中极性共价键与非极性共价键数之比为6︰1C.常温下,11 2 L的甲烷气体中含有的












