(14分)实验室中所用少量氯气是用下列方法制取的 4HCl(浓)+MnO2Cl2↑+MnCl2+2H
| (14分)实验室中所用少量氯气是用下列方法制取的, 4HCl(浓)+MnO2  Cl2↑+MnCl2+2H2O Cl2↑+MnCl2+2H2O试回答下列问题: (1)该反应是氧化还原反应吗? ,如果是氧化还原反应,请指出___ 是氧化剂, 是还原剂,_________是氧化产物,________是还原产物,根据上述氧化还原反应式判断氧化性:______﹥_______;还原性:______﹥_______。 ⑵写出该反应的离子方程式 _________ ⑶用双线桥法标出该反应电子转移的方向和数目 _______________________________ |
参考解答
| . ⑴ 是 MnO2 HCl Cl2 MnCl2 MnO2﹥Cl2 HCl﹥MnCl2 (2)4H++2Cl-+MnO2  Cl2↑+Mn2++2H2O Cl2↑+Mn2++2H2O(3) 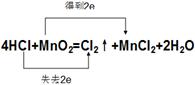 |
试题分析:(1)根据反应的方程式可知,氯元素的化合价从-1价升高到0价,而锰元素的化合价从+4价降低到+2价,所以属于氧化还原反应。其中氧化剂是二氧化锰,HCl是还原剂。氯气是氧化产物,而氯化镁是还原产物。由于在氧化还原反应中氧化剂的氧化性强于氧化产物的,还原剂的还原性强于还原产物的,所以氧化性和还原性强弱顺序分别是MnO2﹥Cl2、HCl﹥MnCl2。 (2)氯化氢和氯化锰都是可以拆开的,所以该反应的离子方程式是 4H++2Cl-+MnO2  Cl2↑+Mn2++2H2O。 Cl2↑+Mn2++2H2O。(3)双线桥中起点和终点的元素是同一种,所以该氧化还原反应的表示是 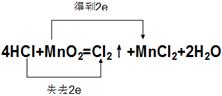 点评:在进行氧化还原反应的有关判断时,关键时准确标出有关元素的化合价变化情况,然后依据有关的概念进行分析判断即可。 |
相似问题
火药是中国的“四大发明”之一 永远值得炎黄子孙骄傲 也永远会激励着我们去奋发图强。黑火药在发生爆炸时
火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S===K2S+2NO2↑+C
已知ICl与锌和水的反应如下:2ICl+2Zn ═ ZnI2+ZnCl2 ICl+H2O ═ HCl
已知ICl与锌和水的反应如下:2ICl+2Zn ═ ZnI2+ZnCl2,ICl+H2O ═ HCl+HIO,下列说法正确的是()A.ZnCl2既是氧化产物又是还原产物B.ZnI2既是
已知NH4CuSO3与足量的1mol·L-1硫酸溶液混合微热 产生下列现象:①有红色金属生成;②有刺
已知NH4CuSO3与足量的1mol·L-1硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法合理的是
(7分).已知:CuI是难溶于水的白色固体。氧化性Cu2+>I2> Cu+ 还原性Cu>I-> Cu
(7分).已知:CuI是难溶于水的白色固体。氧化性Cu2+>I2> Cu+,还原性Cu>I-> Cu+(1)根据物质氧化性还原性的强弱推测,在溶液中Cu2+和I-反应的产物
下列说法正确的是( )。A.反应Na→Na2O→Na2O2中钠元素被连续氧化B.1 mol金属钠发
下列说法正确的是( )。A.反应Na→Na2O→Na2O2中钠元素被连续氧化B.1 mol金属钠发生反应Na→Na2O和发生反应Na→Na2O2转移电子数相等C.1 mol Cl2












