已知常温常压下:① 3Cl2+2NH3→N2+6HCl ②3Cl2+8NH3→N2+6NH4Cl
| 已知常温常压下:① 3Cl2+2NH3→N2+6HCl ,②3Cl2+8NH3→N2+6NH4Cl (1)完成并配平反应③的化学方程式,并标出电子转移方向和数目: ③ 3Cl2+4NH3→ (2)在反应③中:还原剂是 ,还原产物是 。 (3)若按③反应后产生气体4.48 L(标准状况),则被氧化的气体的物质的量是 mol。 |
参考解答
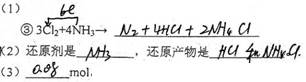 |
| 略 |
相似问题
将6.4g铜和足量浓硝酸反应 Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。
将6 4g铜和足量浓硝酸反应,Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。(1)有多少摩尔硝酸被还原?(2)产生的二氧化氮在标准状况下的体积是多少升?
短周期元素X Y Z在周期表中的位置关系如图所示 已知X最外层电子数为2 则下列叙述中 正确的是 (
短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是()A.Z一定是活泼的金属元素B.Y的最高价氧化物的水化物
氧化还原反应中 水的作用可以是氧化剂 还原剂 既是氧化剂又是还原剂 既非氧化剂又非还原剂等。下列反应
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O===H2SO4+2HBr相比较,水的
下列说法正确的是A.在3NO2+H2O=2HNO3+NO中 氧化剂和还原剂的质量比为1:2B.SO2
下列说法正确的是A.在3NO2+H2O=2HNO3+NO中,氧化剂和还原剂的质量比为1:2B.SO2气体使品红溶液褪色,表现了SO2的氧化性C.浓盐酸和MnO2反应时,浓盐酸中
下列类型的反应 一定有元素化合价发生变化的是( )A化合反应 B分解反应
下列类型的反应,一定有元素化合价发生变化的是()A化合反应 B分解反应 C置换反应 D复分解反应












