六价铬对人体有毒 含铬废水要经过化学处理后才能排放 方法是用绿矾(FeSO4·7H2O)把废水中六价
| 六价铬对人体有毒,含铬废水要经过化学处理后才能排放,方法是用绿矾(FeSO4·7H2O)把废水中六价铬还原成三价铬离子,再加入过量的石灰水,使铬离子生成Cr(OH)3沉淀。 (1)配平下列主要反应的化学方程式。  H2Cr2O7+ H2Cr2O7+ FeSO4+ FeSO4+ H2SO4—— H2SO4—— Fe2(SO4)3+ Fe2(SO4)3+ Cr2(SO4)3+ Cr2(SO4)3+ H2O H2O(2)处理后的沉淀中有Cr(OH)3外,还有__________________ (用化学式表示)。 (3)现在处理1×103 L含铬(+6)78 mg·L-1的废水,需要绿矾_________ g。 |
参考解答
| (1)1 6 6 3 1 7 (2)Fe(OH)3 (3)1 251 |
| 本题考查了氧化还原反应方程式的配平和计算。铬元素的化合价由+6降到+3,铁元素的化合价由+2升高到+3,应用得失电子守恒时要特别注意每个H2Cr2O7含有两个铬原子,再应用观察法配平整个化学方程式。 由H2Cr2O7+6FeSO4+6H2SO4====3Fe2(SO4)3+Cr2(SO4)3+7H2O可知: 2Cr—H2Cr2O7—6FeSO4·7H2O m(FeSO4·7H2O) 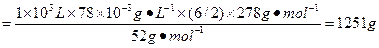 |
相似问题
水热法制备直径为1~100nm的颗粒Y(化合物) 反应原理为:3Fe2++2S2O32-+O2+aO
水热法制备直径为1~100nm的颗粒Y(化合物),反应原理为:3Fe2++2S2O32-+O2+aOH-═Y+S4O62-+2H2O,下列说法中不正确的是( )A.a=4B.将Y均匀分散到
配平下列化学(或离子)方程式:(1)____Cl2 +____KOH→____KCl+____KCl
配平下列化学(或离子)方程式:(1)____Cl2 +____KOH→____KCl+____KClO3 +____H2O (2)____SO32- +____MnO4- +____H+→____Mn2+ +____SO42- +__
KClO3和浓盐酸在一定温度下反应生成二氧化氯.其变化可表述为:(1)完成该化学方程式并配平(未知物
KClO3和浓盐酸在一定温度下反应生成二氧化氯.其变化可表述为:(1)完成该化学方程式并配平(未知物化学式和化学计量数填在划线上).______KClO3+_____
对于反应KMnO4+ HCl——KC1+ MnCl2+Cl2+ H2O(未配平) 若有0.1 mol
对于反应KMnO4+ HCl——KC1+ MnCl2+Cl2+ H2O(未配平),若有0 1 mol KMnO4参加反应,下列说法不正确的是A.被氧化的HCl为0 5 molB.生成0 5 mol
请将5种物质:N2O FeSO4 Fe(NO3)3 HNO3和Fe2(SO4)3分别填入下面对应的横
请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式:(1)_________+__________→__________+___












