氧化还原反应是从______的角度对化学反应进行分类的结果.四种基本反应类型是从______的角度对
氧化还原反应是从______的角度对化学反应进行分类的结果.四种基本反应类型是从______的角度对化学反应进行分类的结果.这二者的关系如下图:图中方框内区域表示所有的化学反应,大圈内区域表示氧化还原反应,大圈外区域表示非氧化还原反应,其中A~D分别表示四种基本反应类型.请分别填写出: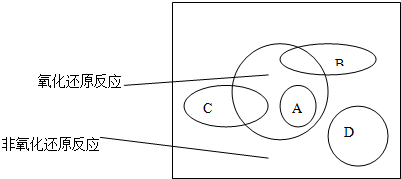 (1)化学反应可以分为哪四种基本类型______、______、______、______. (2)若图中B圈表示化合反应,则C圈表示______反应(填反应所属的基本类型,下同),A圈表示______反应,D圈表示______反应. (3)B圈与氧化还原反应重叠的阴影部分表示的反应,必须满足的条件是______.C圈与氧化还原反应重叠的阴影部分表示的反应,必须满足的条件是______.请分别举出符合以上两种情况的一例:______,______. (4)下列说法正确的是______. A.置换反应一定属于氧化还原反应 B.有单质参加和有单质生成的化学反应一定是氧化还原反应 C.属于氧化还原反应的化合反应必定是因为有单质参与了反应 D.氧化还原反应发生的本质是化合价发生了变化. |
参考解答
| 分类标准不一样,化学反应的分类结果就不一样,根据化合价是否发生变化,可以将化学反应分为氧化还原反应和非氧化还原反应;根据反应物、生成物的种类及其变化,可以将化学反应分为:化合反应、分解反应、置换反应、复分解反应,故答案为:化合价是否发生变化;反应物、生成物的种类及其变化; (1)根据反应物、生成物的种类及其变化,可以将化学反应分为:化合反应、分解反应、置换反应、复分解反应,故答案为:化合反应;分解反应;置换反应;复分解反应; (2)部分化合反应属于氧化还原反应,部分分解反应属于氧化还原反应,所有的置换反应均是氧化还原反应,所有的复分解反应均不是氧化还原反应,故答案为:分解;置换;复分解; (3)B、C圈表示的反应部分是氧化还原反应,所以是化合反应和分解反应两种情况,故答案为:有元素化合价变化的化合反应;有元素化合价变化的分解反应;4Na+O2=2Na2O; 2KClO3
(4)A、置换反应一定是氧化还原反应,故A正确; B、有单质参加和有单质生成的化学反应如3O2═3O3,不属于氧化还原反应,故B错误; C、属于氧化还原反应的化合反应不一定均有单质参与了反应,比如SO2+H2O2=H2SO4,故C错误; D、氧化还原反应发生的本质是电子的转移,故D错误. 故选A. |
相似问题
将SO2通入CuSO4和NaCl的浓溶液中 溶液颜色变浅 析出白色沉淀 取该沉淀分析 知其中含Cl:
将SO2通入CuSO4和NaCl的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀分析,知其中含Cl:35 7%,Cu:64 3%,SO2在上述反应中作用是( )A.酸B.漂
将NaClO3和Na2SO3按物质的量比2:1加入烧瓶中 再滴入少量H2SO4溶液并用水溶解 加热
将NaClO3和Na2SO3按物质的量比2:1加入烧瓶中,再滴入少量H2SO4溶液并用水溶解、加热,产生棕黄色气体X,反应后测得NaClO3和Na2SO3恰好完全反应.则X为(
下列化学反应属于氧化还原反应且水既不作氧化剂又不作还原剂的是( )A.CaO+H2O=Ca(OH)
下列化学反应属于氧化还原反应且水既不作氧化剂又不作还原剂的是( )A.CaO+H2O=Ca(OH)2B.NaH+H2O=NaOH+H2↑C.3NO2+H2O=2HNO3+NOD.2H2O+2F2=4HF+O2↑
氮化铝(AlN)具有耐高温 抗冲击 导热性好等优良性质 被广泛应用于电子工业 陶瓷工业等领域.在一定
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C
单晶硅是制作电子集成电路的基础材料.科学家预计 到2011年一个电脑芯片上将会集成10亿个晶体管 其
单晶硅是制作电子集成电路的基础材料.科学家预计,到2011年一个电脑芯片上将会集成10亿个晶体管,其功能远比我们想象的要大的多,这对硅的纯度要求很高












