【化学——选修3:物质结构与性质】(15分) 人类文明的发展历程 也是化学物质的认识和发现的历程 其
| 【化学——选修3:物质结构与性质】(15分) 人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化碳、聚乙烯、二氧化硅等17种“分子”改变过人类的世界。 (1)铁原子在基态时,价电子(外围电子)排布式为______________________________。 (2)硝酸钾中NO 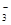 的空间构型为________,写出与NO 的空间构型为________,写出与NO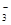 互为等电子体的一种非极性分子化学式____________________________________。 互为等电子体的一种非极性分子化学式____________________________________。(3)6氨基青霉烷酸的结构如图所示,其中采用sp3杂化的原子有____________。 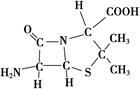 (4)下列说法正确的有________(填字母序号)。 a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高 b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价 c.聚乙烯(┌└CH2CH2┐ ┘n)分子中有5n个σ键 d.由下表中数据可确定在反应Si(s)+O2(g)===SiO2(s)中,每生成60 g SiO2放出的能量为(2c-a-b) kJ
 |
参考解答
| (1)3d64s2 (2)平面正三角形 SO3 (BF3、BBr3等) (3)C、N、O、S (4)a (5)8Fe+2NH3  2Fe4N+3H2, 2Fe4N+3H2,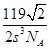 |
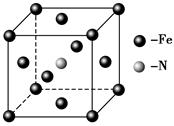
试题分析:(2)NO为平面正三角形结构,中心原子为sp2杂化,利用增减电子的方法,确定等电子体。 (3)形成的化学键都是σ键的中心原子均采用sp3杂化。 (5)晶胞中铁原子数:8× 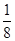 +6× +6×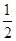 =4,氮原子数为1,故产物的化学式为Fe4N。 =4,氮原子数为1,故产物的化学式为Fe4N。两个最近的Fe原子间的距离为s cm(是面上对角线的一半),晶胞棱长为 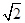 s cm,密度为 s cm,密度为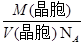 = =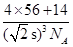 g·cm-3= g·cm-3=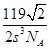 g·cm-3。 g·cm-3。 |
相似问题
天然存在的金属钫(Fr)极微量。它的21种已知同位素都有放射性。它是碱金属元素中最重的元素。根据它
天然存在的金属钫(Fr)极微量。它的21种已知同位素都有放射性。它是碱金属元素中最重的元素。根据它在周期表中的位置预言其性质,其中不正确的是( )A
运用元素周期律分析下面的推断 其中错误的是 ( )A.砹(85号元素)是一种有色固体 HAt应该不
运用元素周期律分析下面的推断,其中错误的是 ( )A.砹(85号元素)是一种有色固体,HAt应该不稳定,且AgAt是有色难溶于水固体B.铍(Be)是一种金属,
下图是元素周期表前四周期的一部分 关于元素R W X Y Z的叙述正确的是( )A.最高价氧化物的
下图是元素周期表前四周期的一部分,关于元素R、W、X、Y、Z的叙述正确的是( )A.最高价氧化物的水化物的酸性:W>YB.Z的单质常温下是液体,所在的周
(12分)根据下列某些短周期元素中元素性质回答问题。 ①②③④⑤⑥⑦⑧⑨⑩原子半径/10 -10
(12分)根据下列某些短周期元素中元素性质回答问题。 ①②③④⑤⑥⑦⑧⑨⑩原子半径 10 -10m 0 371 860 741 430 771 100 991 520 750 71最高价
能说明氯的非金属性比硫强的事实是( )A.氯气与氢气反应生成氯化氢 而硫与氢气反应生成硫化氢B.
能说明氯的非金属性比硫强的事实是()A.氯气与氢气反应生成氯化氢,而硫与氢气反应生成硫化氢B.向硫化氢的水溶液中通入氯气可得到淡黄色的硫C.氯气能












