(10分)下图是元素周期表短周期中11种元素的化台价与原子序数的关系示意图 请回答下列问题(用具体的
(10分)下图是元素周期表短周期中11种元素的化台价与原子序数的关系示意图,请回答下列问题(用具体的元素符号作答):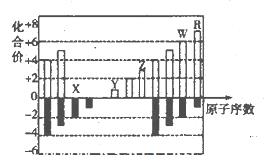 (1)元素x、Y、z、W、R五种元素中属于金属元素的是___________;Z的简单离子的结构示意图是___________。 (2)由此图可以判断,11种元素中处于同主族的共有____________组。 (3)X、Y.Z三种元素的原子半径大小顺序为___________;它们的离子的半径大小顺序为____________。 |
参考解答
(1)Na、Al;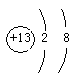 ; ;(2)4 (3)Na>Al>O;O2->Na+>Al3+ |
试题分析:(1)从化合价及原子序数上判断,X是O元素,Y是Na元素,Z是Al元素,W是S元素,R是Cl元素,所以这5种元素中属于金属元素的是Na、Al;Al3+的原子核内有13个质子,核外有10个电子,离子结构示意图为 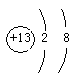 ; ;(2)依据同主族元素的化合价规律判断,最高正价与负价分别完全相同的元素属于同主族,但O常见- 2价,与S同主族;F无正价,与Cl同主族,所以共有4组属于同主族的元素; (3)O、Na、Al的原子半径的比较依据电子层数越多,原子半径越大,核电荷数越少原子半径越大,三者的原子半径的大小顺序是Na>Al>O;三者的离子结构相同,所以离子半径的大小依据核电荷数越少,离子半径越大,所以离子半径的大小顺序是O2->Na+>Al3+ |
相似问题
(18分)运用物质结构的知识完成下列问题。(1)第一电离能介于B N之间的第二周期元素有
(18分)运用物质结构的知识完成下列问题。(1)第一电离能介于B、N之间的第二周期元素有(填元素符号)。(2)配离子[TiCl(H2O)5]2+的中心离子化合价为
下列结论不正确的是A粒子半径:S>S2->Cl-B氢化物沸点:H2O>HF>HClC结合质子能力:O
下列结论不正确的是A粒子半径:S>S2->Cl-B氢化物沸点:H2O>HF>HClC结合质子能力:OH->SiO>COD离子还原性:S2->I->Br-
(15分)A B D E F为短周期元素 非金属元素A最外层电子数与其周期数相同 B的最外层电子数是
(15分)A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B 在D中充分燃烧能生成其最高价化合
下列化学用语中 不正确的是A.氯原子结构示意图: B.HCl的电子式:C.H2O分子的结构式:H-O
下列化学用语中,不正确的是A.氯原子结构示意图: B.HCl的电子式:C.H2O分子的结构式:H-O-HD.乙炔的比例模型:
A B C D E F为短周期六种元素 原子序数依次增大 其中A与E同主族且能形成离子化合物EA B
A、B、C、D、E、F为短周期六种元素,原子序数依次增大,其中A与E同主族且能形成离子化合物EA,B与F同主族,E与F同周期。D的核电荷数是B的最外层电子数2倍












