将15.6g Na2O2与2.7g Al粉混合后 投入足量的水中 充分反应(设能产生的气体全部放出)
| 将15.6g Na2O2与2.7g Al粉混合后,投入足量的水中,充分反应(设能产生的气体全部放出)。 (1)Na2O2与水反应的化学方程式为 ,15.6g Na2O2在该反应中转移电子的物质的量为 mol。 (2)反应结束时生成的气体在标准状况下为 L。 (3)取a g Na2O2与Al粉组成的混合物,放入适量的水中,固体完全溶解,在标准状况下 放出气体V L,则V的取值范围是 (用含a的代数式表示,结果可不化简)。 |
参考解答
| (1)(2分)2Na2O2+2H2O=4NaOH+O2↑;(2分)0.2mol (2)(2分)5.6L (3)(4分) 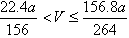 |
| 15.6g Na2O2的物质的量为0.2mol;2.7g Al的物质的量为0.1mol; (1)Na2O2与水反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑;1mol Na2O2与水反应转移的电子数为1mol;所以,15.6g Na2O2在该反应中转移电子的物质的量为0.2mol; (2)15.6g Na2O2与水反应生成0.4mol氢氧化钠,生成0.1mol氧气;生成的氢氧化钠与AL反应的方程式为: 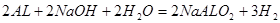 ,所以2.7g Al粉反应后生成氢气0.15mol;所以反应结束时生成的气体在标准状况下为5.6L; ,所以2.7g Al粉反应后生成氢气0.15mol;所以反应结束时生成的气体在标准状况下为5.6L;(3) 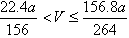 |
相似问题
(16分)某同学想通过下图装置(夹持装置已略去)实验 探究SO2与Na2O2反应的产物. Ⅰ.装置B
(16分)某同学想通过下图装置(夹持装置已略去)实验,探究SO2与Na2O2反应的产物. Ⅰ.装置B的作用.装置D的作用.Ⅱ.如何检验反应中是否有O2生成.
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质 有关说法不正确
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是()A.铝钠合金是混合物B.铝钠合金若投入
(8分)某校化学兴趣小组 通过下列装置探究Na2CO3和NaHCO3的热稳定性 设计如下的探究方案
(8分)某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。(1)提出假设:Na2CO3或NaHCO3加热
(1)除去混入NaCl溶液中少量NaHCO3杂质的试剂是 离子方程式为
(1)除去混入NaCl溶液中少量NaHCO3杂质的试剂是 ,离子方程式为。(3分)(2)除去Na2CO3粉末中混入的NaHCO3杂质用________方法,化学方程式为。(3分)
(8分)“套管实验”是将一支较小的玻璃仪器装入另一支玻璃仪器中 经组装来完成原来需要较多仪器进行的实
(8分)“套管实验”是将一支较小的玻璃仪器装入另一支玻璃仪器中,经组装来完成原来需要较多仪器进行的实验。因其具有许多优点,已被广泛应用于化学实验












