根据下图所示的实验过程和提供的数据 下列判断不正确的是( )A.I中未变质的NaOH质量为5.3g
根据下图所示的实验过程和提供的数据,下列判断不正确的是( )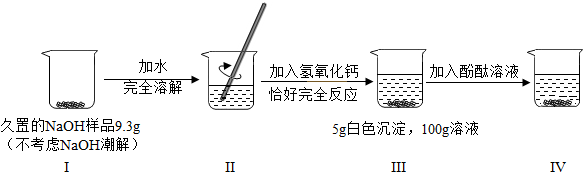
|
参考解答
| 由样品溶液加入氢氧化钙生成 沉淀可知氢氧化钠已变质,则II中溶液有氢氧化钠、碳酸钠两种溶质,B正确; 碳酸钠和氢氧化钙恰好反应生成碳酸钙沉淀和氢氧化钠,则IV中溶液是氢氧化钠溶液,能使酚酞变红,D正确; 设样品中碳酸钠的质量为x,生成氢氧化钠的质量为y Ca(OH)2+Na2CO3═CaCO3↓+2NaOH 106 100 80 x 5g y
由此可知:I中未变质的NaOH质量为9.3g-5.3g=4g,故A错误; III中溶液溶质的质量分数是:
故选A. |
相似问题
某校研究性学习小组要制取少量的氢气 实验室提供一瓶未标明质量分数的稀硫酸和必要的仪器.研究小组取含杂
某校研究性学习小组要制取少量的氢气,实验室提供一瓶未标明质量分数的稀硫酸和必要的仪器.研究小组取含杂质的锌粒32 5g,与100g该稀硫酸刚好完全反应,
一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是(
一定质量的镁条在氧气中完全燃烧后生成氧化镁.固体质量随时间的变化关系如图所示.下列说法不正确的是( )A.生成MgO的质量:m2gB.参加反应的Mg的
某校化学兴趣小组的同学为了制取氢氧化镁 他们取9.5gl氯化镁固体全部溶解在40.5g水中制成不饱和
某校化学兴趣小组的同学为了制取氢氧化镁,他们取9 5gl氯化镁固体全部溶解在40 5g水中制成不饱和溶液,然后向其中加入55 8g某溶质质量分数的氢氧化钠溶液
某混合物只含有CaCO3和CaO 测得其中钙元素的质量分数为50%.取该混合物16g充分煅烧后 将剩
某混合物只含有CaCO3和CaO,测得其中钙元素的质量分数为50%.取该混合物16g充分煅烧后,将剩余固体投入水中,固体全部溶解,则溶液中溶质的质量为(
现有82g含有杂质的氧化铜样品 与氢气充分反应 得到纯铜65g 水18.14g 其中样品中的杂质不与
现有82g含有杂质的氧化铜样品,与氢气充分反应,得到纯铜65g,水18 14g,其中样品中的杂质不与氢气反应;试计算该样品中氧化铜的质量分数是______;样品












