已知反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0。某温度下 将2 mol SO2和
已知反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是 ( ) 2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是 ( )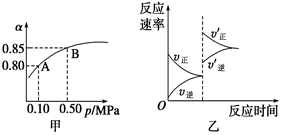 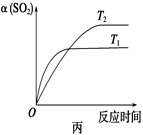
|
参考解答
| C |
A错,A点SO2的物质的量为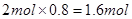 ,即SO2的平衡浓度为1.6 mol/L;B错,平衡时SO2的物质的量为 ,即SO2的平衡浓度为1.6 mol/L;B错,平衡时SO2的物质的量为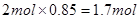 ,SO3的物质的量为0.3mol,O2的物质的量为0.85mol,在恒容容器中,B点SO2、O2、SO3的平衡浓度之比为1.7∶0.85∶0.3;C正确;D错,由图可知温度在 ,SO3的物质的量为0.3mol,O2的物质的量为0.85mol,在恒容容器中,B点SO2、O2、SO3的平衡浓度之比为1.7∶0.85∶0.3;C正确;D错,由图可知温度在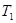 时达平衡时间更短,所以温度大小关系为T1>T2 时达平衡时间更短,所以温度大小关系为T1>T2 |
相似问题
在一定温度下 密闭容器中可逆反应A(g)+3B(g) 2C(g)达到平衡的标志是( )A.C的生
在一定温度下,密闭容器中可逆反应A(g)+3B(g) 2C(g)达到平衡的标志是()A.C的生成速率与B的反应速率相等 B.单位时间内生成n molA,同时生成3n mol
一定条件下 将NO2与SO2以体积比1:2置于密闭容器中发生NO2(g)+SO2(g)SO3(g)+
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生NO2(g)+SO2(g)SO3(g)+NO(g)的可逆反应,下列能说明反应达到平衡状态的是A.体系压强保持不变B.混
(6分)在一容积为2L且容积不变的密闭容器中加入适量碳粉和0.2molH2O。在800℃条件下 经2
(6分)在一容积为2L且容积不变的密闭容器中加入适量碳粉和0 2molH2O。在800℃条件下,经20s后达到如下化学平衡:C(s) +H2O(g) CO(g) + H2(g);△H="
(10分)830K时 在密闭容器中发生下列可逆反应:CO(g)+H2O(g)CO2(g)+H2(g)
(10分)830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)CO2(g)+H2(g) △H<0试回答下列问题:(1)若起始时c(CO)="2" mol·L-1,c(H2O
(8分)硫酸生产中 SO2催化氧化成SO3的热化学方程式为:2 SO2 (g)+ O2(g)2 SO
(8分)硫酸生产中,SO2催化氧化成SO3的热化学方程式为:2 SO2 (g)+ O2(g)2 SO3(g)△H =" —196 0" kJ.mol-1①容器体积不变时,为了提高SO2












