在一定温度下 密闭容器中可逆反应A(g)+3B(g) 2C(g)达到平衡的标志是( )A.C的生
在一定温度下,密闭容器中可逆反应A(g)+3B(g) 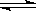 2C(g)达到平衡的标志是( ) 2C(g)达到平衡的标志是( )A.C的生成速率与B的反应速率相等 B.单位时间内生成n molA,同时生成3n molB C.A、B、C的浓度不再变化 D.A、B、C的浓度之比为1:3:2 |
参考解答
| C |
| 可逆反应达到平衡的本质为:体系内各组分的浓度保持不变,正反应速率与逆反应速率相等;所以 A错,C的生成速率与C的反应速率相等时反应才平衡;B错,每时每刻均这样反应;C正确;D错,平衡后各组分的浓度不变,但一定浓度比为化学计量数比; |
相似问题
一定条件下 将NO2与SO2以体积比1:2置于密闭容器中发生NO2(g)+SO2(g)SO3(g)+
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生NO2(g)+SO2(g)SO3(g)+NO(g)的可逆反应,下列能说明反应达到平衡状态的是A.体系压强保持不变B.混
(6分)在一容积为2L且容积不变的密闭容器中加入适量碳粉和0.2molH2O。在800℃条件下 经2
(6分)在一容积为2L且容积不变的密闭容器中加入适量碳粉和0 2molH2O。在800℃条件下,经20s后达到如下化学平衡:C(s) +H2O(g) CO(g) + H2(g);△H="
(10分)830K时 在密闭容器中发生下列可逆反应:CO(g)+H2O(g)CO2(g)+H2(g)
(10分)830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)CO2(g)+H2(g) △H<0试回答下列问题:(1)若起始时c(CO)="2" mol·L-1,c(H2O
(8分)硫酸生产中 SO2催化氧化成SO3的热化学方程式为:2 SO2 (g)+ O2(g)2 SO
(8分)硫酸生产中,SO2催化氧化成SO3的热化学方程式为:2 SO2 (g)+ O2(g)2 SO3(g)△H =" —196 0" kJ.mol-1①容器体积不变时,为了提高SO2
(19分)高炉炼铁中发生的基本反应之一如下:FeO(s)+ CO (g) Fe(s)+ CO2(g
(19分)高炉炼铁中发生的基本反应之一如下:FeO(s)+ CO (g) Fe(s)+ CO2(g)△H>0 (1)此反应的平衡常数表达式为:K=;(2)温度升高,达到新的平衡












