在一定条件下 密闭容器中可发生可逆反应:N2(g) + 3H2(g) 2NH3(g) 。下列说法中
在一定条件下,密闭容器中可发生可逆反应:N2(g) + 3H2(g) 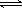 2NH3(g) 。 2NH3(g) 。下列说法中,表明这一反应已经达到化学平衡状态的是
|
参考解答
| B |
正确答案:B 化学平衡状态:在一定条件下,当一个可逆反应的正反应速率与逆反应速率相等时,反应物的浓度与生成物的浓度不再改变,达到一种表面静止的状态,即'化学平衡状态'. 其中,正反应速率与逆反应速率相等是化学平衡状态的实质,而反应物的浓度与生成物的浓度不再改变是化学平衡状态的表现。 A、不正确,N2、H2、NH3的浓度相等,不能说明反应物的浓度与生成物的浓度不再改变; B.正确,N2、H2、NH3的浓度不再变化; C.不正确,N2、H2、NH3在密闭容器中共存只能说明反应没有完全进行; D.不正确,反应仍在进行,正、逆反应速率相等,但不等于零。 |
相似问题
(7分)在0.1L密闭容器中有0.1molSO2和0.05molO2发生反应 恒温下30min后达到
(7分)在0 1L密闭容器中有0 1molSO2和0 05molO2发生反应,恒温下30min后达到平衡。(1)若得到0 06molSO3,求达平衡时SO2的浓度;(2)求30min内的反应
一定温度下恒容的密闭容器中 反应A2(g)+B2(g) 2AB(g)达到平衡的标志是A.正反应速率和
一定温度下恒容的密闭容器中,反应A2(g)+B2(g) 2AB(g)达到平衡的标志是A.正反应速率和逆反应速率相等且都为零B.容器内气体的总压强不随时间变化C.单
(8分)(2009·山东卷)运用化学反应原理研究氮 氧等单质及其化合物的反应有重要意义。(1)合成氨
(8分)(2009·山东卷)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。(1)合成氨反应N2(g)+3H2(g) ===2NH3(g),若在恒温、恒压条件下向平
在10 L密闭容器中 把10 mol M和10 mol N混合发生如下反应:3M(g)+N(g)
在10 L密闭容器中,把10 mol M和10 mol N混合发生如下反应:3M(g)+N(g) xP(g)+2Q(g),当反应达到平衡时,生成4 mol Q,并测得P的平衡浓度为0 4
已经建立化学平衡的某可逆反应 当条件改变时化学平衡向正反应方向移动 下列叙述正确的是①生成物的质量分
已经建立化学平衡的某可逆反应,当条件改变时化学平衡向正反应方向移动,下列叙述正确的是①生成物的质量分数一定增加 ②生成物的产量一定增加 ③反应












