有A B C D四种短同期元素 最高正价依次为+1 +4 +5 +7 其核电荷数按B C A D的顺
| 有A、B、C、D四种短同期元素,最高正价依次为+1、+4、+5、+7,其核电荷数按B、C、A、D的顺序增大.已知B、C的次外层电子数为2,D、A的次外层电子数均为8,且A、D原子的电子层数相同.请回答: (1)写出A、B、C、D的元素符号:A______、B______、C______、D______. (2)画出A的原子结构示意图:______; (3)写出AD的电子式:______; (4)写出A、C的最高价氧化物对应水化物相互反应的化学方程式:______. |
参考解答
| (1)短周期元素的最高化合价等于族序数,所以A在ⅠA族、B在ⅣA族、C在ⅤA族、D在ⅤⅡA族,又A、D的次外层电子数为8,则A、D均为第三周期元素,A为Na、D为Cl;B、C的次外层电子数为2,在第二周期,所以B为C、C为N. 故答案为:Na、C、N、Cl; (2)A为Na,核外有三个电子层,电子数分别为2、8、1,原子结构示意图为 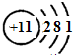 , 故答案为: 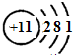 ; (3)AD为氯化钠,是离子化合物,电子式中氯离子应用中括号括起来且右上角标出所带电荷,电子式为 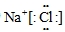 , 故答案为: 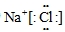 ; (4)A、C的最高价氧化物对应的水化物分别为NaOH、HNO3,二者反应生产NaNO3和H2O,反应的方程式为NaOH+HNO3═NaNO3+H2O, 故答案为:NaOH+HNO3═NaNO3+H2O. |
相似问题
短周期主族元素W X Y Z的原子序数依次增大 W X原子的最外层电子数之比为4:3 Z原子比X原子
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是( )A.W、Y、Z的
短周期元素甲 乙 丙 其中甲 乙两元素原子的最外层电子数分别是次外层电子数的2倍和3倍 丙元素的最高
短周期元素甲、乙、丙,其中甲、乙两元素原子的最外层电子数分别是次外层电子数的2倍和3倍,丙元素的最高正价和最低负价的代数和等于4.则下列判断不正确
A B C三种元素的原子具有相同的电子层数 它们相同物质的量的原子获得相同物质的量的电子时释放出的能
A、B、C三种元素的原子具有相同的电子层数,它们相同物质的量的原子获得相同物质的量的电子时释放出的能量是A>C>B,则它们核电荷数大小顺序是( )A
X Y为两种元素的原子 X的阴离子与Y的阳离子具有相同的电子层结构 由此可知( )A.X的原子半径
X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,由此可知( )A.X的原子半径大于Y的原子半径B.X的电负性大于Y的电负性C.X阴离
有A B C D E五种短周期元素 它们的核电荷数按C A B D E的顺序增大.C D都能分别与A
有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E的顺序增大.C、D都能分别与A按原子个数比为1:1或2:1形成化合物;CB可与EA2反应生成C2A












