已知A为常见的金属单质 根据图示的关系 回答下列问题.(1)确定A B C D的化学式 A为____
| 已知A为常见的金属单质,根据图示的关系,回答下列问题. (1)确定A、B、C、D的化学式,A为______,B为______,C为______,D为______, (2)在上述①~⑧的反应中属于非氧化还原反应的有______. (3)写出下列反应的化学(或离子)方程式: D→C(写离子方程式)______; E→F(写化学方程式)______. 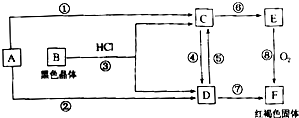 |
参考解答
| B是黑色晶体,应为Fe3O4,它与HCl反应生成FeCl2和FeCl3,红褐色固体F为Fe(OH)3,则E为Fe(OH)2,C为FeCl2,D为FeCl3,所以A为Fe, (1)由以上分析可知A为Fe,B为Fe3O4,C为FeCl2,D为FeCl3,故答案为:Fe;Fe3O4;FeCl2;FeCl3; (2)在上述①~⑧的反应中①、②、⑧有单质参加反应,肯定为氧化还原反应,④、⑤为FeCl2和FeCl3之间的转化,化合价发生变化,为氧化还原反应,③、⑥、⑦没有化合价发生变化,不是氧化还原反应, 故答案为:③、⑥、⑦; (3)D→C转化可由FeCl3与Fe反应生成FeCl2,反应的离子方程式为2Fe3++Fe═3Fe2+, E→F为Fe(OH)2与氧气反应生成,反应的化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3, 故答案为:2Fe3++Fe═3Fe2+;4Fe(OH)2+O2+2H2O═4Fe(OH)3. |
相似问题
如图为反应Fe+CuSO4═FeSO4+Cu中电子转移的关系图 则图中的元素甲 乙分别表示( )A
如图为反应Fe+CuSO4═FeSO4+Cu中电子转移的关系图,则图中的元素甲、乙分别表示( )A.FeCuB.CuSC.FeOD.FeS
离子反应是中学化学中重要的反应类型.回答下列问题:(1)在发生离子反应的反应物或生成物中 一定存在_
离子反应是中学化学中重要的反应类型.回答下列问题:(1)在发生离子反应的反应物或生成物中,一定存在______.①单质 ②氧化物 ③电解质 ④盐 ⑤化
下列情况下的酸既表现出强氧化性 又表现了酸性的是( )A.常温下将木炭加入浓硫酸中B.氧化亚铁(F
下列情况下的酸既表现出强氧化性,又表现了酸性的是( )A.常温下将木炭加入浓硫酸中B.氧化亚铁(FeO)加入稀硝酸C.常温下将铜粉加入浓硝酸中D.氧
氧化还原反应中 水的作用可以是氧化剂 还原剂 既是氧化剂又是还原剂 既非氧化剂又非还原剂等.下列反应
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等.下列反应与Br2+SO2+2H2O═H2SO4+2HBr相比较,水的作用
氮化钠和氢化钠与水反应的化学方程式如下:Na3N+3H2O→3NaOH+NH3 NaH+H2O→Na
氮化钠和氢化钠与水反应的化学方程式如下:Na3N+3H2O→3NaOH+NH3,NaH+H2O→NaOH+H2↑.有关Na3N和NaH的叙述正确的是( )A.离子半径:Na+>N3->H+B












