镁是海水中含量较多的金属 镁 镁合金及其镁的化合物在科学研究和工业生产中用途非常广泛。(1)Mg2N
| 镁是海水中含量较多的金属,镁、镁合金及其镁的化合物在科学研究和工业生产中用途非常广泛。 (1)Mg2Ni是一种储氢合金,已知: Mg(s) + H2(g)=MgH2(s) △H1=-74.5kJ·mol-1 Mg2Ni(s) + 2H2(g)=Mg2NiH4(s) △H2=-64.4kJ·mol-1 Mg2Ni(s)+2MgH2(s) = 2Mg(s)+Mg2NiH4(s) △H3 则△H3 = kJ·mol-1。 (2)工业上可用电解熔融的无水氯化镁获得镁。其中氯化镁脱水是关键工艺之一,一种正在试验的氯化镁晶体脱水的方法是:先将MgCl2·6H2O转化为MgCl2·NH4Cl·nNH3(铵镁复盐),然后在700℃脱氨得到无水氯化镁,脱氨反应的化学方程式为 ;电解熔融氯化镁,阴极的电极反应式为 。 (3)储氢材料Mg(AlH4)2在110-200°C的反应为:Mg(AlH4)2=MgH2 +2A1+3H2↑每生成27gAl转移电子的物质的量为 。 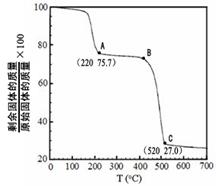 (4)工业上用MgC2O4·2H2O热分解制超细MgO,其热分解曲线如图。 图中隔绝空气条件下B→C发生反应的化学方程式为 。 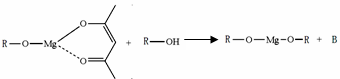 (5)一种有机镁化合物可用于制造光学元件的涂布液,化学式可表示为: 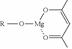 ,它可发生如下反应: ,它可发生如下反应:ROH与B的核磁共振氢谱如下图: 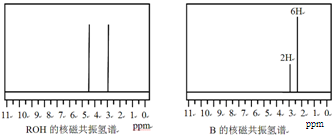 ROH由C、H、O、F四种元素组成的含氟有机物,分子中只有1个氧原子,所有氟原子化学环境相同,相对分子质量为168,则ROH的结构简式为 ; B的结构简式为 。 |
参考解答
(1)+84.6(2分)。 (2)MgCl2·NH4Cl·nNH3 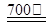 MgCl2 +(n+1)NH3↑ + HCl↑ (2分); Mg2++2e-= Mg(2分)。 MgCl2 +(n+1)NH3↑ + HCl↑ (2分); Mg2++2e-= Mg(2分)。(3)3mol(2分)。(4)MgC2O4 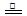 MgO + CO↑+ CO2↑(2分) MgO + CO↑+ CO2↑(2分)(5)(CF3)2CHOH (2分); 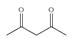 (2分)。 (2分)。 |
试题分析:(1)方程式②-①×2=-64.4-(-74.5)×2=+84.6 kJ·mol-1;(2)化合物分解得到无水氯化镁、氨气、和氯化氢;阴极阳离子放电;(3)该反应中只有铝元素化合价降低,由+3价到0价,生成1mol铝,电子转移3mol;(4)根据图数据计算分析,若总质量为148g,第一次分解产物质量为148×75.7%=112g,第二次分解产物的质量为148×27%=40g,所以A点生成MgC2O4,C点生成MgO;B→C发生反应为MgC2O4 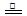 MgO + CO↑+ CO2↑;(5)根据信息含有1个羟基,图谱中显示物质中含有2中化学环境的氢且数目相同,即物质中只含有两个氢原子,其它全被氟取代,根据相对分子质量确定为(CF3)2CHOH。 MgO + CO↑+ CO2↑;(5)根据信息含有1个羟基,图谱中显示物质中含有2中化学环境的氢且数目相同,即物质中只含有两个氢原子,其它全被氟取代,根据相对分子质量确定为(CF3)2CHOH。 |
相似问题
关于反应3Cl2 + 6KOH KClO3 + 5KCl + 3H2O 以下说法正确的是A.KOH
关于反应3Cl2 + 6KOH KClO3 + 5KCl + 3H2O,以下说法正确的是A.KOH既不是氧化剂,又不是还原剂B.Cl2是氧化剂,KOH是还原剂 C.3mol氯气参加反
现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液 整个过程中含碘物质的物质的量与所加入KBr
现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示。请回答下列问题:(1)b点时,K
在一定条件下 NO跟NH3可以发生反应:6NO+4NH3=5N2+6H2O 关于该反应下列说法中不正
在一定条件下,NO跟NH3可以发生反应:6NO+4NH3=5N2+6H2O,关于该反应下列说法中不正确的是( )A.H2O既不是氧化产物也不是还原产物B.该反应中被氧化
(本题16分)无水AlCl3可用作有机合成的催化剂 食品膨松剂等。工业制备无水AlCl3的流程如下:
(本题16分)无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业制备无水AlCl3的流程如下:(1)氯化炉中通入O2的目的是 _________。(2)氯化炉中Al
氧化还原反应是有元素化合价发生改变的化学反应 氧化还原反应的本质是_______________。在
氧化还原反应是有元素化合价发生改变的化学反应,氧化还原反应的本质是_______________。在氧化还原反应中,还原剂_________电子,本身发生____________












