(9分)下图为周期表中的一部分。已知A B C D均为短周期元素 A与D原子序数之和为C原子序数的1
(9分)下图为周期表中的一部分。已知A、B、C、D均为短周期元素,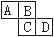 A与D原子序数之和为C原子序数的1.5倍。 (1)B元素符号是: _______、D在元素周期表中第_______族。 (2)四种元素中原子半径最大的是(填元素符号)_______,B、C、D三种离子中半径最大的是(填离子符号)_______。 (3)B比C的氢化物的沸点高是因为_____ __;A、D两元素的气态氢化物相互反应的生成物的电子式: ,其中存在_______键、_______(填“极性”或“非极性”)共价键。 (4)写一个离子方程式证明C和D的非金属性相对强弱: 。 |
参考解答
(1)O;ⅦA族;(2)S;S2-;(3)水分子间有氢键;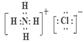 离子、极性; 离子、极性;(4)S2-+Cl2=S↓+2Cl- |
| 试题分析:假设B的原子序数是a,则A是a-1,C是a+8,D是a+9.根据题意可得(a-1)+(a+9)= 1.5(a+8)。解得a=8,所以这几种元素分别是:A是N;B是O;C是S;D是Cl。(1)B元素符号是O;D在元素周期表中第ⅦA族;(2)同一周期的元素,原子序数越大,原子半径越小;不同周期的元素,原子核外电子层数越多,原子半径就越大。所以这四种元素中原子半径最大的是S。电子层结构相同的微粒,核电荷数越大,离子半径就越小;电子层结构不同的微粒,离子核外电子层数越多,离子半径就越大,所以B、C、D三种离子中半径最大的是S2-;(3)O和S是同族元素,它们的氢化物的结构相似,而沸点H2O的比H2S高是因为水分子间有氢键,增加了分子之间的相互吸引,使物质汽化消耗的能量高;A、D两元素的气态氢化物相互反应的生成物NH4Cl的电子式是 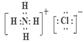 。其中存在离子键、极性共价键;(4)活动性强的元素的单质能够把活动性弱的元素从化合物中置换出来,证明C和D的非金属性相对强弱的一个离子方程式是:S2-+Cl2=S↓+2Cl-。 。其中存在离子键、极性共价键;(4)活动性强的元素的单质能够把活动性弱的元素从化合物中置换出来,证明C和D的非金属性相对强弱的一个离子方程式是:S2-+Cl2=S↓+2Cl-。 |
相似问题
四种主族元素的离子a Xm+ bYn+ cZn-和dRm-(a b c d为元素的原子序数) 它们具
四种主族元素的离子a Xm+,bYn+,cZn-和dRm-(a,b,c,d为元素的原子序数),它们具有相同的电子层结构,若m>n,对下列叙述的判断正确的是( )①a-
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半 该元素( ) A.在自然界中只
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素( )A.在自然界中只以化合态的形式存在B.单质常用作半导体材料和光导纤维C.最
(10分)下表为元素周期表中的一部分.用化学式或元素符号回答下列问题: IAⅡAⅢAⅣAVAⅥAⅦA
(10分)下表为元素周期表中的一部分.用化学式或元素符号回答下列问题:IAⅡAⅢAⅣAVAⅥAⅦA02⑥⑦3①③⑤⑧⑩4②④⑨(1)10种元素中,化学性质最不活
下列叙述错误的是( )A.13C和14C属于同一种元素 它们互为同位素B.1H和2H是不同的核素
下列叙述错误的是( )A.13C和14C属于同一种元素,它们互为同位素B.1H和2H是不同的核素,它们的质子数相等C.14C和14N的质量数相等,它们的中子数不等
下列说法正确的是A.元素周期表中一共有7个周期和18个族B.金属元素的原子最外层电子数一定都小于4C
下列说法正确的是A.元素周期表中一共有7个周期和18个族B.金属元素的原子最外层电子数一定都小于4C.质量数不同的两种原子,一定不互为同位索D.主族元












