已知:还原性HSO3->I- 氧化性IO3-> I2。在含 0.3 mol NaHSO3的溶液中逐滴
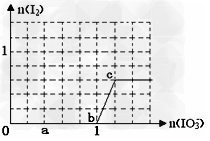
| 已知:还原性HSO3->I-,氧化性IO3-> I2。在含 0.3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如图所示。下列说法不正确的是 |
 |
| [ ] |
| A.0~b间的反应可用如下离子方程式表示:3HSO3- + IO3-=3SO42- + I- + 3H+ B.a点时消耗NaHSO3的物质的量为0.12 mol C.b点时的还原产物可能是KI或NaI,b~c间的还原产物是I2 D.当溶液中I-与I2的物质的量之比为5∶2时,加入的KIO3为0.18mol |
参考解答
| D |
相似问题
下列排列顺序完全正确的组合是①溶解性:Na2CO3>NaHCO3>AgCl>AgI②氧化性:MnO2
下列排列顺序完全正确的组合是①溶解性:Na2CO3>NaHCO3>AgCl>AgI②氧化性:MnO2>Cl2>Fe3+>Cu2+③常温下,α1、α2、α3分别表示pH=2的盐酸、pH=12
高铁酸钾(K2FeO4)是一种既能杀菌 消毒 又是絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程
高铁酸钾(K2FeO4)是一种既能杀菌、消毒,又是絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式为:Fe(OH)3+ ClO-+OH-→FeO42-+Cl-+H2O(未配平)
向含有Cu(NO3)2 Zn(NO3)2 Fe(NO3)3 AgNO3各0.1 mol的混合溶液中加
向含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0 1mol的混合溶液中加入0 1mol铁粉,充分搅拌后,Fe溶解,溶液中不存在Fe3+,同时析出0 1molAg。下列结论
某反应中反应物与生成物有:AsH3 H2SO4 KBrO3 K2SO4 H3AsO4 H2O和一种未
某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X (1)已知KBrO3在反应中得到电子,则该反应的还原剂是_____________
已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol Na2O2(s)+C
已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ mol Na2O2(s)+CO2(g)=Na2CO3(s)+12O2(g);△H=-226kJ mol根据以上热化学方程式判断,下列说法正确












