某反应中反应物与生成物有:AsH3 H2SO4 KBrO3 K2SO4 H3AsO4 H2O和一种未
| 某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X. (1)已知KBrO3在反应中得到电子,则该反应的还原剂是______________________. (2)已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为______________. (3)根据上述反应可推知________________. a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3 c.还原性:AsH3>X d.还原性:X>AsH3 (4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:______+_____ |
参考解答
| (1)AsH3 (2)Br2 (3)ac (4) 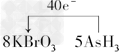 |
相似问题
已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol Na2O2(s)+C
已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ mol Na2O2(s)+CO2(g)=Na2CO3(s)+12O2(g);△H=-226kJ mol根据以上热化学方程式判断,下列说法正确
某学习小组探究浓 稀硝酸氧化性的相对强弱的 按下图装置进行试验(夹持仪器已略去).实验表明浓硝酸能将
某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去).实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此得出的
根据下列反应:(1)2Fe3++2I-=2Fe2++I2 (2)Br2+2Fe2+=2Br-+2Fe
根据下列反应:(1)2Fe3++2I-=2Fe2++I2(2)Br2+2Fe2+=2Br-+2Fe3+,判断离子的还原性由强到弱的顺序是( )A.Br->I->Fe2+B.I->Fe2+>Br-C.Fe2+>I->Br-D.Br->Fe2+>I-
下列叙述正确的是( )A.发生化学反应时失去电子越多的金属原子 还原能力越强B.金属阳离子被还原后
下列叙述正确的是( )A.发生化学反应时失去电子越多的金属原子,还原能力越强B.金属阳离子被还原后,一定得到该元素的单质C.某物质只含一种元素,
有下列氧化还原反应:①Fe+CuSO4═Cu+FeSO4 ②Cu+2FeCl3═CuCl2+2FeC
有下列氧化还原反应:①Fe+CuSO4═Cu+FeSO4 ②Cu+2FeCl3═CuCl2+2FeCl2③2FeCl2+Cl2═2FeCl3根据上述反应可判断各粒子氧化性由强到弱的顺序正确的是(












