含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感。(1)过碳酸钠是一种有多种用途的新型氧系固
| 含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感。 (1)过碳酸钠是一种有多种用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。 ①H2O2有时可作为矿业废液消毒剂,如消除采矿业废液中的氰化物(如NaCN),经以下反应实现:NaCN+H2O2+H2O=A+NH3↑,则生成物A的化学式______________ ②某强酸性反应体系中,反应物和生成物共六种物质: O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→ O2。 写出该反应的离子方程式:_______________________________________________。 (2)某天然碱的化学式可表示为:aNa2CO3·bNaHCO3·2H2O,取m g天然碱溶于水配成溶液,再向溶液中逐滴加入1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系某同学作出了如图所示的A和B曲线,试回答下列问题: 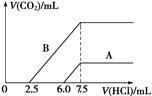 ①_______曲线正确,天然碱的化学式为___________, ②加盐酸后产生CO2气体体积(标准状况)的最大值为 _____________mL。 (3) 常温下用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2可生成0.5 mol N2,则y=_______________。 |
参考解答
| (1)①NaHCO3 ②2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑ (2)B; Na2CO3·NaHCO3·2H2O, 112 (3)3 |
试题分析:(1)①化学反应的过程就是原子重新组合的过程。在这个过程中,元素的种类及原子个数不变。可得A化学式为:NaHCO3。该反应中H2O2只发生了如下过程:H2O2→ O2。H2O2失去电子,作还原剂,则还有氧化剂MnO4-,反应后该微粒转化为Mn2+.结合原子守恒和电子守恒。可得离子方程式是:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑。(2) ①Na2CO3与盐酸反应分步进行。首先发生:Na2CO3+HCl='NaCl+' NaHCO3.当Na2CO3完全转化为NaHCO3后,发生NaHCO3+HCl=NaCl+H2O+CO2↑。若固体只含有Na2CO3,则前后两步消耗的盐酸物质的量相等。由于某天然碱的化学式可表示为:aNa2CO3·bNaHCO3·2H2O,还含有NaHCO3,故放出气体消耗的盐酸要比前半部分多。故B曲线正确。n(Na2CO3)=' 1' mol/L×2. 5×10-3L=2. 5×10-3 mol.n(NaHCO3)总='1' mol/L×5×10-3L=5×10-3 mol。所以原固体产生的碳酸氢钠的物质的量为:n(NaHCO3)= 5×10-3 mol-2. 5×10-3 mol.= 2. 5×10-3 mol。n(Na2CO3):n(NaHCO3)=1:1.所以某天然碱的化学式可表示为: Na2CO3·NaHCO3·2H2O。②n(CO2)= n(Na2CO3)+n(NaHCO3)= 5×10-3 mol.V(CO2)= n(CO2)·Vm=5×10-3 mol×22.4mol/L×103ml/L='112ml.' (3)根据质量守恒定律可得2Y+X='8' 讨论求解得:X=2,Y=3.物质化学式成立。 |
相似问题
下列离子方程式书写正确的是A.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+ H2OB.标
下列离子方程式书写正确的是A.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+ H2OB.标准状况下将112ml氯气通入6ml 1mol L的碘化亚铁溶液中3Cl2+2Fe2++4I-=
下列离子方程式正确的是A.用Fe除去FeCl2溶液中的少量的FeCl3杂质:Fe+Fe3+=2Fe2
下列离子方程式正确的是A.用Fe除去FeCl2溶液中的少量的FeCl3杂质:Fe+Fe3+=2Fe2+B.实验室制取NO2:Cu+4H++2=Cu2++2NO2↑+2H2OC.硫酸溶液与
下列相关离子方程式的书写正确的是A.铁溶于适量硝酸中:B.向水中通入少量氯气:C.碳酸氢钠溶液中加入
下列相关离子方程式的书写正确的是A.铁溶于适量硝酸中:B.向水中通入少量氯气:C.碳酸氢钠溶液中加入过量D.硫酸溶液中加入过量溶液:
下列离子方程式 正确的是A.等物质的量的SO2与氢氧化钠溶液反应:SO2+OH-=HSO3-B.用食
下列离子方程式,正确的是A.等物质的量的SO2与氢氧化钠溶液反应:SO2+OH-=HSO3-B.用食醋除去水瓶中的水垢:CO32-+2CH3COOH=2CH3COO-+CO2+H2OC.已知电
进行污水处理分析时 常用双硫腙(H2Dz 二元弱酸)把金属离子络合成电中性的物质 再用CCl4萃取络
进行污水处理分析时,常用双硫腙(H2Dz,二元弱酸)把金属离子络合成电中性的物质,再用CCl4萃取络合物,从而把金属离子从水溶液中完全分离出来。如用双硫腙(H2












