(14分)连二亚硫酸钠(Na2S2O4)俗称保险粉 是一种强还原剂 广泛用于纺织工业。其制备过程如下
| (14分)连二亚硫酸钠(Na2S2O4)俗称保险粉,是一种强还原剂,广泛用于纺织工业。其制备过程如下: ①把甲酸(HCOOH)和足量的NaOH溶液混合; ②用Na2SO3固体和某酸反应制备SO2气体; ③在一定温度下,将足量的SO2气体通入①的溶液中,即有保险粉生成,同时生成一种气体。 (1)写出NaOH的电子式 (2)制备SO2时所选用的酸,你认为下列最适宜选用的是
(4)保险粉可以用于除去废水中的重铬酸根离子(Cr2O72-被转化为Cr3+),这是目前除去酸性废水中铬离子的有效方法之一,则每消耗0.1mol保险粉,理论上可以除去Cr2O72-的物质的量为 mol。 (5)保险粉不稳定,容易分解生成甲、 乙、 丙三种化合物。若将甲、乙两种物质分别配成溶液,在甲溶液中加入稀硫酸,则有淡黄色沉淀和气体丙产生;乙溶液中加入BaCl2溶液和稀盐酸,有气体丙产生,但无白色沉淀。 在甲溶液中加入稀硫酸后所发生反应的离子方程式为 保险粉分解的化学方程式为 (6)保险粉在空气中容易吸收氧气而发生氧化。其方程式为: ①2Na2S2O4+O2+H2O==4NaHSO3或②2Na2S2O4+O2+H2O==4NaHSO3+NaHSO4 请设计实验证明氧化时发生的是②的反应。 |
参考解答
| (共14分,每空2分) (1) 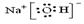 (2) B (2) B (3) NaOH+HCOONa+2SO2==Na2S2O4+CO2+H2O(写HCOOH且配平,也给分) (4) 0.1 (5) S2O32-+2H+==SO2+S↓+H2O 2 Na2S2O4 ='=' Na2S2O3+Na2SO3+SO2 (6) 取少许固体溶于水中,加入BaCl2溶液,有白色沉淀产生,则证明是② (或取少许固体溶于水中,若闻到刺激性气味,则证明是②) |
试题分析:(1)见答案。 (2)浓盐酸有挥发性,若选用浓盐酸则制得的SO2不纯,若选用稀硝酸,则SO2会被硝酸氧化,若选用稀硫酸,则反应速率较慢,且生成的SO2易溶于水,所以最合适的试剂是B。(3)步骤①所得溶液为HCOONa和NaOH的混合溶液,Na2S2O4中硫的化合价为+3价,由SO2生成Na2S2O4时硫元素化合价降低而被还原,则还原剂为HCOONa(碳的化合价为+2价),氧化产物为CO2,反应物和生成确定后配平并补写生成物水,即得化学方程式:NaOH+HCOONa+2SO2==Na2S2O4+CO2+H2O。(4)除去废水中的重铬酸根离子时保险粉作还原剂,被氧化为SO42-,每摩尔保险粉失6mol电子,而每摩尔Cr2O72-得6mol电子,所以每消耗0.1mol保险粉,理论上可以除去Cr2O72-的物质的量为0.1mol。(5) +3价的硫酸不稳定,容易发生歧化反应,根据甲与稀硫酸的反应情况可判断甲为Na2S2O3,根据乙与BaCl2溶液反应的情况可判断乙为Na2SO3,丙为SO2,故甲溶液中加入稀硫酸后所发生反应的离子方程式为S2O32-+2H+==SO2+S↓+H2O;保险粉分解的化学方程式为2Na2S2O4 ='=' Na2S2O3+Na2SO3+SO2。(6)反应②的生成物有NaHSO4,要证明发生的反应是②而不是①,只需检验SO42-即可,具体实验是:取少许固体溶于水中,加入BaCl2溶液,有白色沉淀产生,则证明是②(注:NaHSO3不与BaCl2溶液反应)。 |
相似问题
(15分)废旧碱性锌锰干电池内部的黑色物质A主要含有MnO2 NH4Cl ZnCl2 还有少量的Fe
(15分)废旧碱性锌锰干电池内部的黑色物质A主要含有MnO2、NH4Cl、ZnCl2,还有少量的FeCl2和炭粉,用A制备高纯MnCO3的流程图如下。(1)碱性锌锰干电池的负
下列表示对应化学反应的离子方程式正确的是A.向铁粉中加入足量稀硝酸:2Fe+6H+=2Fe3++3H
下列表示对应化学反应的离子方程式正确的是A.向铁粉中加入足量稀硝酸:2Fe+6H+=2Fe3++3H2↑B.向AlCl3溶液中滴加浓氨水至过量:Al3++4OH-=AlO2-
下列关于常温下电解质溶液的叙述中 正确的是A.碳酸氢铵溶液和足量氢氧化钠溶液混合的离子反应:B.向一
下列关于常温下电解质溶液的叙述中,正确的是A.碳酸氢铵溶液和足量氢氧化钠溶液混合的离子反应:B.向一定体积一定物质的量浓度的氨水中滴加盐酸,所得
下列离子方程式正确的是A.钠与水反应:Na+2H2O=Na+ +2OH- + H2↑B.硅酸钠溶液与
下列离子方程式正确的是A.钠与水反应:Na+2H2O=Na+ +2OH- + H2↑B.硅酸钠溶液与醋酸溶液混合:SiO3 2-+2H+=H2SiO3↓C.0 01mol L NH4Al(SO4)2 溶
下列离子方程式正确的是( )A.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO-B.双氧水
下列离子方程式正确的是( )A.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO-B.双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2OC.用铜作电极电解












