Ⅰ.A B C D为前四周期元素。A元素的原子价电子排布为ns2np2 B元素原子的最外层电子数是其
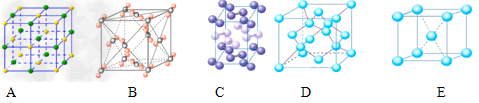
| Ⅰ.A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素原子的最外层电子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子。请回答下列问题: ⑴当n=2时,AB2属于_______分子(填“极性”或“非极性”),分子中有_______个π键。A6H6分子中A原子的杂化轨道类型是_______杂化。 ⑵当n=3时,A与B形成的晶体属于_______晶体。 ⑶若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是_______(用元素符号表示)。 Ⅱ.⑴下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是__________(请用相应的编号填写) |
 |
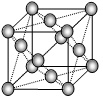
| ⑵①与N2O互为等电子体的阴离子为______________(填一种即可);②根据价层电子对互斥模型确定ClO3-离子的空间构型为______________。 ⑶已知某红紫色配合物的组成为CoCl3·5NH3·H2O,该配合物中的中心离子钴离子在基态时的核外电子排布式为___________。 ⑷下图是金属铝晶体结构的示意图。已知金属铝的密度为2.7g/cm3,则紧邻的铝原子的半径为_____________cm。(已知 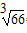 =4.04) =4.04) |
 |
参考解答
| Ⅰ⑴非极性;2;sp2; ⑵原子; ⑶P>S>Si Ⅱ⑴BC;⑵①SCN-或N3-; ②三角锥形;⑶ [Ar3d6; ⑷1.42×10-8 |
相似问题
锌是一种重要的金属 锌及其化合物有着广泛的应用.①指出锌在周期表中的位置:第______周期 第__
锌是一种重要的金属,锌及其化合物有着广泛的应用.①指出锌在周期表中的位置:第______周期,第______族,属于______区.②葡萄糖酸锌[CH2OH(CHOH)4CO
下列说法正确的是( )①具有规则几何外形的固体一定是晶体 ②NaCl晶体中与每个Na+距
下列说法正确的是( )①具有规则几何外形的固体一定是晶体 ②NaCl晶体中与每个Na+距离相等且最近的Na+共有12个③非极性分子中一定含有非极性键 ④
下列分子中属于含有极性键的非极性分子 且分子中各原子最外层都满足8电子稳定结构的是( )A.CH4
下列分子中属于含有极性键的非极性分子,且分子中各原子最外层都满足8电子稳定结构的是( )A.CH4B.PCl3C.SiCl4D.XeF4
用一带静电的有机玻璃棒靠近A B两种纯液体的细流 现象如图所示。据此分析A B两种液体分子的极性正确
用一带静电的有机玻璃棒靠近A、B两种纯液体的细流,现象如图所示。据此分析A、B两种液体分子的极性正确的是 [ ]A A是极性分子,B是非极性分子 B A是非
在BrCH=CHBr分子中 C-Br键采用的成键轨道是( )A.sp-pB.sp2-sC.sp2-
在BrCH=CHBr分子中,C-Br键采用的成键轨道是( )A.sp-pB.sp2-sC.sp2-pD.sp3-p












