氢元素与其他元素形成的二元化合物称为氢化物 下面关于氢化物的叙述正确的是( )
氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )
|
参考解答
| B |
| 考查的知识点:原子结构、物质结构、元素周期律 A:氢元素有三种常见同位素:H((1H)、D(21H)、T(31H);D2O的中子数为 (2-1)×2+(16-8)=10。所以A错 B:结构式可以从电子式去演变,也可以根据各原子形成的共价键个数去书写 N原子形成三个共价键,H原子形成一个共价键,所以NH3的结构式为H— 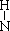 —H —H是正确的 C、书写电子式之前一定要先判断是离子键还是共价键 判断的原理:一般金属与非金属元素间形成离子键,除了AlCl3等 一般非金属元素与非金属元素间形成共价键,除了铵盐等 从上可知,HCl中H和Cl之间形成的是共价键而非离子键,正确的电子式为H 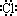 所以C错 D、元素的非金属性越强,气态氢化物越稳定。由非金属活动性顺序表 F、Cl、Br、I、S(从F到S,元素的非金属性逐渐减弱)可知: 非金属性:I> S 氢化物的稳定性:HI > H2S ,所以D错误 |
相似问题
下列说法中 正确的是( )A.键长越长 化学键越牢固B.成键原子间原子轨道重叠越少 共价键越牢
下列说法中,正确的是( )A.键长越长,化学键越牢固B.成键原子间原子轨道重叠越少,共价键越牢固C.对双原子分子来讲,键能越大,含有该键的分
下列各组微粒中不属于等电子体的是 A.CH4 NH4+B.H2S HClC.CO2 N2OD.CO3
下列各组微粒中不属于等电子体的是A.CH4、NH4+B.H2S、HClC.CO2、N2OD.CO32-、NO3-
(10分)A B C D E F六种物质在一定条件下有如下图所示的相互转化关系 所有反应物和生成物均
(10分)A、B、C、D、E、F六种物质在一定条件下有如下图所示的相互转化关系,所有反应物和生成物均已给出。(1)若反应①、②、③均为溶液中的置换反应,
由A B元素组成的含4个原子核和42个电子的-2价阳离子中 1个A的核内质子数比B的核内质子数多8个
由A、B元素组成的含4个原子核和42个电子的-2价阳离子中,1个A的核内质子数比B的核内质子数多8个,试通过计算确定:(1)A、B元素名称分别为和。(2)写出
意大利科学家合成了一种新型的氧分子 其化学式为O4。下列关于O4说法正确的是A.一个分子O4有两个分
意大利科学家合成了一种新型的氧分子,其化学式为O4。下列关于O4说法正确的是A.一个分子O4有两个分子O2构成B.O4是一种单质C.等质量的O4和O2含有相同数












