已知某化合物是由钙 钛 氧三种元素组成的晶体 其晶胞结构如图所示 则该物质的化学式为( )A.Ca
已知某化合物是由钙、钛、氧三种元素组成的晶体,其晶胞结构如图所示,则该物质的化学式为( )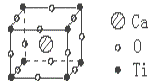
|
参考解答
| A |
试题分析:利用均摊法确定化学式,处于晶胞中心的原子被一个晶胞占有,处于顶点上的原子被8个晶胞占有,处于棱上的原子被4个晶胞占有。所以钙原子有一个,钛原子的个数为 8×1/8-=1,氧原子的个数为12×1/4=3个,故该物质的化学式为CaTiO3,所以本题选择A。 点评:本题考查了晶胞的计算,本题要掌握处于晶胞中心的原子被一个晶胞占有,处于顶点上的原子被8个晶胞占有,处于棱上的原子被4个晶胞占有,而处于面上的原子为2个晶胞占有,本题比较简单。 |
相似问题
下列各组物质中 含有离子晶体 分子晶体 原子晶体各一种的是( )A.KCl H2SO4 SB.金
下列各组物质中,含有离子晶体、分子晶体、原子晶体各一种的是( )A.KCl、H2SO4、SB.金刚石、Na3PO4、MgC.NH4F、SiO2、ArD.H2O、干冰、SiO2
下列物质的熔点高低顺序 正确的是A.金刚石>晶体硅>碳化硅B.K>NaC.NaF<NaCl<NaBr
下列物质的熔点高低顺序,正确的是A.金刚石>晶体硅>碳化硅B.K>NaC.NaF<NaCl<NaBrD.CI4>CBr4
Ⅰ下列描述中正确的是( )A.CS2为V形的极性分子B.的空间构型为平面三角形C.SF6中有6对
Ⅰ下列描述中正确的是()A.CS2为V形的极性分子B.的空间构型为平面三角形C.SF6中有6对完全相同的成键电子对D.SiF4和的中心原子均为sp3杂化Ⅱ 金属镍
下列物质中 属于分子晶体的是( )①二氧化硅 ②碘 ③食盐 ④蔗糖 ⑤磷酸A.②④⑤B.①②④C.
下列物质中,属于分子晶体的是( )①二氧化硅 ②碘 ③食盐 ④蔗糖 ⑤磷酸A.②④⑤B.①②④C.②③④⑤D.①②③⑤
NaF NaI MgO均为离子化合物 根据下列数据 这三种化合物的熔点高低顺序是:( )物质①
NaF、NaI、MgO均为离子化合物,根据下列数据,这三种化合物的熔点高低顺序是:( )物质①NaF②NaI③MgO离子电荷数112键长(10-10m)2 313 182 10A.①>②>












