已知原子序数依次增大的A B C D E五种元素中有2种为非金属元素 其原子序数均小于30。其中A
| 已知原子序数依次增大的A、B、C、D、E五种元素中有2种为非金属元素,其原子序数均小于30。其中A、B、C、E的价电子层中均有2个未成对电子,A、B同族且可以形成原子个数比为1:1的化合物BA,属于原子晶体。回答下列问题: (1)在地壳中A、B元素的含量的关系为 大于 (用元素符号回答)。 (2)AO2和BO2分别为A和B的最高价氧化物,两种氧化物中含有π键的物质的电子式 为 。从原子半径大小的角度分析,A或B与氧原子形成π键难易程度的差异 。 (3)C元素在元素周期表中的位置为 ,其最高化合价为 。C单质晶体的堆积方式为 ,每个晶胞中实际占有C原子的个数为 。 (4)D与E同族且不相邻,D存在D2+和D3+两种常见离子,它们与K+及CN-能形成一种可溶性蓝色化合物,用作染料。它的结构单元如图所示,则在该晶体中n(CN-):n(K+):n(D3+):n(D2+)= ,该蓝色化合物可以由D3+与K4〔D(CN)6〕制得,也可由D2+与K3〔D(CN)6〕制得。请写出K4〔D(CN)6〕与Cl2反应生成K3〔D(CN)6〕的化学方程式 。  |
参考解答
(1)Si(1分)、C(1分) (2)  (2分),Si的原子半径较大,Si、O原子间距离较大,p-p轨道肩并肩重叠程度较小,不易形成稳定的π键而C恰好相反。(2分,其他合理答案均给分) (2分),Si的原子半径较大,Si、O原子间距离较大,p-p轨道肩并肩重叠程度较小,不易形成稳定的π键而C恰好相反。(2分,其他合理答案均给分)(3)第4周期ⅣB族(1分)+4(1分)六方最密堆积(1分)2(2分) (4)6:1:1:1(2分)2 K4[Fe(CN)6 + Cl2 ='=' 2KCl + 2 K3[Fe (CN)6 (2分) |
试题分析:⑴A、B、C、E的价电子层中均有2个未成对电子,A、B同族且可以形成原子个数比为1:1的化合物BA,属于原子晶体。可以判断为SiC,在地壳中A、B元素的含量的关系为Si大于C。⑵二氧化硅中不存在π键,π键只存在于二氧化碳中。Si的原子半径较大,Si、O原子间距离较大,p-p轨道肩并肩重叠程度较小,不易形成稳定的π键而C恰好相反。⑶C一定是金属,且原子序数比硅的要大,因此只能是第二十二号元素钛。位于周期表中的第4周期ⅣB族,失去最外层四个电子显正四价,钛单质的堆积方式为六方紧密堆积,每个晶胞中实际占有钛原子的个数为2。⑷依据均摊法,在该结构单元中,三价D离子与二价D离子的数目是一样的,都为  个,而氰根离子为: 个,而氰根离子为: ,再根椐电荷守恒,可知钾离子应该为: ,再根椐电荷守恒,可知钾离子应该为: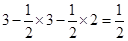 ,可知在该晶体中n(CN-):n(K+):n(D3+):n(D2+)=6︰1︰1︰1 ,可知在该晶体中n(CN-):n(K+):n(D3+):n(D2+)=6︰1︰1︰1 |
相似问题
已知A B C D E F六种短周期元素的性质或结构信息如下表 请根据信息回答下列问题。元素性质或结
已知A、B、C、D、E、F六种短周期元素的性质或结构信息如下表,请根据信息回答下列问题。元素性质或结构信息A单质常温下为固体,难溶于水易于溶CS2。能形
(每空1分 共10分)根据已学知识 请你回答下列问题: (1)含有8个质子 10个中子的原子的化学符
(每空1分,共10分)根据已学知识,请你回答下列问题: (1)含有8个质子,10个中子的原子的化学符号__________。(2)最外层电子排布为4s24p1的原子的
A B C D4种元素 A单质在B单质中燃烧发出苍白色火焰 C单质跟A D形成化合物的水溶液反应生成
A,B,C,D4种元素,A单质在B单质中燃烧发出苍白色火焰,C单质跟A,D形成化合物的水溶液反应生成A单质,C原子与B原子的电子层结构相同,且最外层电子数之
X Y Z和W代表原子序数依次增大的4种短周期元素 它们满足以下条件:①元素周期表中Z与Y相邻 Z与
X,Y,Z和W代表原子序数依次增大的4种短周期元素,它们满足以下条件:①元素周期表中Z与Y相邻,Z与W也相邻; ②Y,Z和W3种元素的原子最外层电子数之和为
不锈钢的种类很多 其中一种铁元素以外 还含有较多的Cr(铬) Ni(镍) Mo(钼) 少量的Si(硅
不锈钢的种类很多,其中一种铁元素以外,还含有较多的Cr(铬)、Ni(镍)、Mo(钼),少量的Si(硅)、C(碳),微量的S(硫)、P(磷)。(1)上述元素中属于第












