某碳酸钠固体样品中含有少量氯化钠.研究性学习小组的同学在探究该固体混合物中碳酸钠的质量分数时 设计并
| 某碳酸钠固体样品中含有少量氯化钠.研究性学习小组的同学在探究该固体混合物中碳酸钠的质量分数时,设计并完成以下实验. ①取质量为a g的三个烧杯,各盛放质量分数相同的稀盐酸25g; ②向三个烧杯中分别放入质量不同的固体样品; ③充分反应后,称量烧杯和剩余物的质量.实验数据如下表.
求:(1)该固体样品中含碳酸钠的质量分数; (2)所用盐酸溶液的质量分数. |
参考解答
答案:
稀盐酸完全反应的是实验2和3
(1)82.8%
(2)14.6%
解析:
比较实验2和实验3可以知道加入固体样品实验3比实验2多1g而剩余的固体的质量也是1g,所以可以判断实验3中的盐酸完全反应,比较实验1和实验2可以知道实验2加入的固体比实验1中多加了3.4g固体样品,而反应后溶液只增加了2.3g说明实验1中的3.2g样品中的碳酸钠全部发生了反应,所以综合以上的分析可以判断实验2中的盐酸已反应完全,实验2中生成气体的质量为:(a+25g)+6.6g-(a+29.4g)=2.2g
分析可以知道实验1的固体样品恰好完全反应,根据质量守恒定律可以知道生成气体的质量为:(a+25g)+3.2g-(a+27.1g)=1.1g;
设6.6g样品中含碳酸钠的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 1.1g
解得x=2.65g
(1)该固体样品中含碳酸钠的质量分数为:
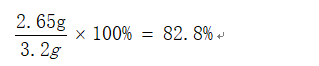
(2)设25g盐酸中含氯化氢的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
73 44
y 2.2g
解得y=3.65g
则盐酸溶液的质量分数为:
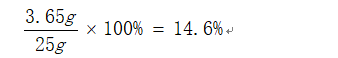
相似问题
某学生称取Na2CO3和NaCl的混合物39.2g 溶于120g水中制成溶液 然后向其中加入94.8
某学生称取Na2CO3和NaCl的混合物39 2g,溶于120g水中制成溶液,然后向其中加入94 8g某质量分数的CaCl2溶液,恰好完全反应,过滤、干燥得到沉淀质量为20g
为了测定石灰石中含CaCO3 的质量分数 取石灰石12.5g 加入盛有100g 稀盐酸的烧杯中 两者
为了测定石灰石中含CaCO3的质量分数,取石灰石12 5g加入盛有100g稀盐酸的烧杯中,两者恰好完全反应(假设杂质不和盐酸反应,也不溶解),烧杯内物质的质
将一块锌投入l00g稀硫酸中 充分反应后 过滤 得到滤液为131.5g 则参加反应的锌的质量为___
将一块锌投入l00g稀硫酸中,充分反应后,过滤,得到滤液为131 5g,则参加反应的锌的质量为______.若将此100g稀硫酸稀释为10%,应加水的质量______.若再
一定量的氢氧化钠溶液中通入CO2 恰好完全反应 所得溶液的质量为53g 溶质的质量分数为20%.求原
一定量的氢氧化钠溶液中通入CO2,恰好完全反应,所得溶液的质量为53g,溶质的质量分数为20%.求原NaOH溶液的质量分数.
为测定某NaCl Na2CO3固体混合物的组成 小明同学取16 g该混合物放入烧杯中 分五次加入稀盐
为测定某NaCl、Na2CO3固体混合物的组成,小明同学取16g该混合物放入烧杯中,分五次加入稀盐酸(每次加入稀盐酸的质量为25g),待反应完全后,得到下面的












