用分子轨道理论说明配合物离子[FeF6]3-和[Fe(CN)6]3-的成键情况。请帮忙给出正确答案和
用分子轨道理论说明配合物离子[FeF6]3-和[Fe(CN)6]3-的成键情况。
请帮忙给出正确答案和分析,谢谢!
参考解答
正确答案:在[FeF63-中Fe3+为d5构型有5个d电子6个F-中有6对孤对电子共17个价电子。因为配体的能量低所以成键分子轨道由配体的12个电子占据而Fe3+的P(325kJ.mol-1)>△o(167kJ.mol-1)所以5个d电子进入非键的t2g轨道和反键的eg*总的排布成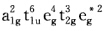 [FeF63是未成对电子数n=5的高自旋配合物。在[Fe(CN)63-中6个CN一提供了6对孤对电子加上Fe3+中5个电子也是17个价电子。由于△o>P这17个电子的排布为a1g2t1u6eg4t2g5形成低自旋配合物。
[FeF63是未成对电子数n=5的高自旋配合物。在[Fe(CN)63-中6个CN一提供了6对孤对电子加上Fe3+中5个电子也是17个价电子。由于△o>P这17个电子的排布为a1g2t1u6eg4t2g5形成低自旋配合物。
在[FeF63-中,Fe3+为d5构型,有5个d电子,6个F-中有6对孤对电子,共17个价电子。因为配体的能量低,所以成键分子轨道由配体的12个电子占据,而Fe3+的P(325kJ.mol-1)>△o(167kJ.mol-1),所以5个d电子进入非键的t2g轨道和反键的eg*,总的排布成,[FeF63是未成对电子数n=5的高自旋配合物。在[Fe(CN)63-中6个CN一提供了6对孤对电子,加上Fe3+中5个电子,也是17个价电子。由于△o>P,这17个电子的排布为a1g2t1u6eg4t2g5,形成低自旋配合物。
相似问题
下列各式中错误的是( )。 ①∫0∞r2R∞Dr=1 ②(θ)sinθdθ=1 ③∫|∮|2dr=1
下列各式中错误的是( )。 ①∫0∞r2R∞Dr=1 ②(θ)sinθdθ=1 ③∫|∮|2dr=1 ④∫0πsinθdθ∫02π|d∮=1 ⑤ ⑥∫0π∫02πY1,02sinθd∮
下列分子中不属于Td点群的是( )。A.SO42-B.PO43-C.ClO4-D.XeF4请帮忙给出
下列分子中不属于Td点群的是( )。A.SO42-B.PO43-C.ClO4-D.XeF4请帮忙给出正确答案和分析,谢谢!
下列分子的键角大小次序正确的是( )。A.NH4+>NH3>H2O>H2SB.NH4+<NH3<H2
下列分子的键角大小次序正确的是( )。A.NH4+>NH3>H2O>H2SB.NH4+<NH3<H2S<H2OC.NH3>NH4+>H2O>H2SD.NH3<NH4+<H2O<H2S请帮忙给出正确答案和分析,谢谢!
HF的第一电离能是16.02eV 而OH基第一电离能是13.2eV 它们的差值几乎与氟原子和氧原子的
HF的第一电离能是16.02eV,而OH基第一电离能是13.2eV,它们的差值几乎与氟原子和氧原子的2p价轨道电离能之间的差值相同,用分子轨道理论解释这个结果。
Cr与CO形成羰基配合物所属的点群是( )。A.D3hB.TdC.OhD.D6h请帮忙给出正确答案和
Cr与CO形成羰基配合物所属的点群是( )。A.D3hB.TdC.OhD.D6h请帮忙给出正确答案和分析,谢谢!












