离子反应是中学化学中重要的反应类型。回答下列问题:(1)在发生离子反应的反应物或生成物中 一定存在有
| 离子反应是中学化学中重要的反应类型。回答下列问题: (1)在发生离子反应的反应物或生成物中,一定存在有 (填序号)。 ①单质;②氧化物;③电解质;④盐;⑤化合物 (2)可用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下图。请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系。   (3)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点。
(4)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“Ba2++SO42-=BaSO4↓”来表示,请写出有关反应的化学方程式(3个): ① ; ② ; ③ 。 |
参考解答
| (1)③⑤ (2) 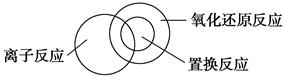 (3)①2CH3COOH+CaCO3=2CH3COO-+Ca2++H2O+CO2↑ ②CH3COOH+OH-=CH3COO-+H2O ③CaCO3+2H+=Ca2++H2O+CO2↑ (4)①BaCl2+H2SO4=BaSO4↓+2HCl ②Ba(OH)2+Na2SO4=BaSO4↓+2NaOH ③NaHSO4+BaCl2=BaSO4↓+HCl+NaCl |
离子反应中一定有离子参与反应或有离子生成,因此一定有电解质(化合物)参与反应或生成。置换反应一定是氧化还原反应,二者有一部分可用离子方程式表示,如Zn+Cu2+=Cu+Zn2+,有的则只能用化学方程式表示,如CuO+H2 Cu+H2O。 Cu+H2O。 |
相似问题
NaNO2是一种食品添加剂 它能致癌。酸性KMnO4溶液与NaNO2的反应方程是:MnO4—+NO2
NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2的反应方程是:MnO4—+NO2—+ Mn2++NO3—+H2O(未配平)。下列叙述中正确的是( )A.该反应中NO2
下列离子方程式的书写与结论均合理的是选项离子方程式结论AAgCl(s) + I-( aq) A
下列离子方程式的书写与结论均合理的是选项离子方程式结论AAgCl(s) + I-( aq) AgI(s) + Cl-(aq)溶解度:AgI > AgClBFe2++ H2O2 +2H+= F
已知HCO3―+AlO2― +H2O=CO32― +Al(OH)3↓;将足量的KHCO3溶液不断滴入
已知HCO3―+AlO2― +H2O=CO32― +Al(OH)3↓;将足量的KHCO3溶液不断滴入含等物质的量的KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与滴入的K
下列反应属于氧化还原反应的是 [ ]A.3NaOH + FeCl3═Fe(OH)3↓+ 3
下列反应属于氧化还原反应的是 [ ]A.3NaOH + FeCl3═Fe(OH)3↓+ 3NaCl B.HCl + NaHCO3==NaCl+H2O+CO2↑ C.Cu + 4HNO3(浓) ==Cu(NO3)2 + 2NO2↑+ 2H2OD.CuCl2+2NaOH==Cu(OH)2↓+2NaCl
下列离子方程式书写正确的是A.在NaClO溶液中通入过量SO2气体:ClO-+H2O+SO2=HCl
下列离子方程式书写正确的是A.在NaClO溶液中通入过量SO2气体:ClO-+H2O+SO2=HClO+HSO3-B.用稀氢碘酸溶液除去铁制品表面的铁锈:Fe2O3+6H+ =2Fe3+ +3H












