工业上制取冰晶石(Na3AlF6)的化学方程式如下 2Al(OH)3+ 12HF+ 3Na2CO3
| 工业上制取冰晶石(Na3AlF6)的化学方程式如下, 2Al(OH)3+ 12HF+ 3Na2CO3=2Na3AlF6+ 3CO2↑+ 9H2O,根据题意完成下列填空: (1)在上述反应的反应物和生成物中,属于非电解质的物质的电子式为 ,属于弱酸的电离方程式 。 (2)上述反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是 (选填编号)。 a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸性 c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢 (3)上述反应物中某些元素处于同一周期。它们最高价氧化物对应的水化物之间发生反应的离子方程式为 。 (4)上述产物当中有一个物质比同族元素类似化合物的沸点高很多,写出这个物质的结构式_______,其沸点较高的原因是_______________;反应物中属于盐的物质中含有的化学键有________________。(填“离子键”或“共价键”或“金属键”) |
参考解答
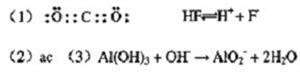 (4)H-O-H,分子间存在氢键,离子键和共价键 |
| 略 |
相似问题
(6分)将32g铜与250mL一定浓度的硝酸恰好完全反应 产生的NO和NO2混合气体在标准状况下的体
(6分)将32g铜与250mL一定浓度的硝酸恰好完全反应,产生的NO和NO2混合气体在标准状况下的体积为11 2L。试计算(1)被还原的HNO3的物质的量mol(2)若反应
在2KMnO4 + 16HCl ='==' 2KCl+2MnCl2十5C12↑+8H2O反应中。(1
在2KMnO4+ 16HCl = "== " 2KCl+2MnCl2十5C12↑+8H2O反应中。(1)在上述反应式用双线桥法标明电子转移的方向和数目。(2若有7 3g HCl被氧化,产生C12的质量为多少克?
某反应中有六种微粒:Co2O3 H2O Cl2 H+ Cl—和Co2+ 已知氧化性:Co2O3>Cl
某反应中有六种微粒:Co2O3、H2O、Cl2、H+、Cl—和Co2+,已知氧化性:Co2O3>Cl2。下列叙述不正确的是( )A.氧化产物为Cl2B.微粒的还原性Cl—>Co2+C.氧
由KClO3与MnO2混合加热 把所得固体加水溶解 过滤后 用硝酸酸化的AgNO3溶液检验滤液中含有
由KClO3与MnO2混合加热,把所得固体加水溶解、过滤后,用硝酸酸化的AgNO3溶液检验滤液中含有Cl-,此过程所发生的反应类型不包含 ( )A.化合反应B.分解
(4分)在Fe3O4 +4CO3Fe+4CO2的的中 是氧化剂
(4分)在Fe3O4 +4CO3Fe+4CO2的的中,是氧化剂,是还原剂,元素被氧化,元素被还原。












