反应:3BrF3+5H2O→HBrO3+Br2+O2+9HF中氧化剂是______ 还原剂是____
| 反应:3BrF3+5H2O→HBrO3+Br2+O2+9HF中氧化剂是______,还原剂是______,氧化产物是______,还原产物是______,被还原的元素是______.请用单线桥法标出该反应中电子转移的方向和数目. |
参考解答
| 在氧化还原反应中,得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,还原剂对应的产物是氧化产物,氧化剂对应的产物是还原产物,得电子化合价降低的元素被氧化, 所以3BrF3+5H2O→HBrO3+Br2+O2+9HF中,溴元素的化合价由+3价变为0价和+5价,氧元素的化合价由-2价变为0价,所以氧化剂是BrF3,还原剂是BrF3和H2O,氧化产物是HBrO3、O2,还原产物是Br2,被还原的元素是+3价的溴,该反应中,部分溴失电子部分得电子,水中氧元素失电子,转移电子数是6, 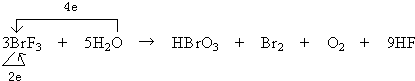 , ,故答案为:BrF3,BrF3、H2O,HBrO3、O2,Br2, 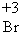 , ,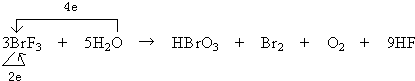 . . |
相似问题
在Fe3O4+4CO高温.3Fe+4CO2的反应中 ______是氧化剂 ______是还原剂 被氧
在Fe3O4+4CO高温 3Fe+4CO2的反应中,______是氧化剂,______是还原剂,被氧化的元素是______,被还原的元素是______.
现有一未配平的氧化还原反应:KClO3+PH3+H2SO4→K2SO4+H3PO4+H2O+X 请回
现有一未配平的氧化还原反应:KClO3+PH3+H2SO4→K2SO4+H3PO4+H2O+X,请回答下列问题(1)该反应的还原剂是______(2)已知0 2molKClO3在反应中得到1mol电
下列物质在一定条件下能够与硫发生反应 且硫作还原剂的是( )A.O2B.FeC.H2D.Zn
下列物质在一定条件下能够与硫发生反应,且硫作还原剂的是( )A.O2B.FeC.H2D.Zn
过氧化氢在二氧化锰催化作用下分解放出氧气的反应机理如下:①MnO2+H2O2+2H+=Mn2++O2
过氧化氢在二氧化锰催化作用下分解放出氧气的反应机理如下:①MnO2+H2O2+2H+=Mn2++O2↑+2H2O②Mn2++H2O2=MnO2+2H+下列说法正确的是( )A.H2O2在①中
属于非氧化还原反应的是( )A.分解反应B.复分解反应C.吸热反应D.银镜反应
属于非氧化还原反应的是( )A.分解反应B.复分解反应C.吸热反应D.银镜反应












