有一种工业废水 其中含有大量的硫酸亚铁 少量的银离子以及污泥.某同学设计了一个既经济又合理的方法回收
| 有一种工业废水,其中含有大量的硫酸亚铁,少量的银离子以及污泥.某同学设计了一个既经济又合理的方法回收银和硫酸亚铁晶体.方案流程如下: |
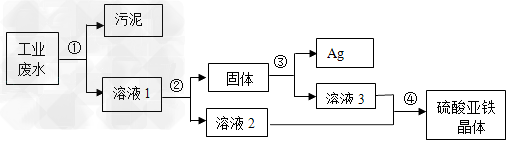 |
| 回答下列问题: (1)步骤②中:需加入的物质是 _________ ,分离所得混合物的方法是 _________ . (2)步骤③中:需加入的物质是 _________ ,发生反应的化学方程式是 _________ . (3)某同学认为经过步骤②后所得固体就是纯净的银,不需要进行步骤③,你认为是否合理? _________ ,理由是 _________ . (4)步骤④的操作是 _________ ,溶液2和溶液3为什么要混合? _________ . |
参考解答
| (1)Fe;过滤 (2)稀硫酸;Fe+H2SO4=FeSO4+H2↑ (3)不合理;因为要使Ag+完全置换出来,必须加入过量的铁. (4)蒸发结晶;两种滤液中都含有硫酸亚铁,可得到更多的硫酸亚铁,综合利用 |
相似问题
下列物质之间的转化能够实现的是( )A.CuOc高温CuO2△CuOB.CaCO3HClCaCl2
下列物质之间的转化能够实现的是( )A.CuOc高温CuO2△CuOB.CaCO3HClCaCl2HNO3Ca(NO3)2C.FeO2点燃Fe2O3HClFeCl3D.Al2O3H2OAl(OH)3HClAlCl3
下表提供的四组物质符合图示 相连物质间在一定条件下可以发生反应的是 [ ]A A B B
下表提供的四组物质符合图示,相连物质间在一定条件下可以发生反应的是 [ ]A、A B、BC、C D、D
工业“从海水中提取镁”的流程图如图:请根据图示回答以下问题:(1)过滤操作需要的玻璃仪器有漏斗 __
工业“从海水中提取镁”的流程图如图:请根据图示回答以下问题:(1)过滤操作需要的玻璃仪器有漏斗、______、玻璃棒.(2)滤液b中含有H2O、______等物
在酸性条件下 次氯酸钠(NaClO) 过氧化氢(H2O2)都有很强的氧化性 可将Fe2+氧化为Fe3
在酸性条件下,次氯酸钠(NaClO)、过氧化氢(H2O2)都有很强的氧化性,可将Fe2+氧化为Fe3+;在溶液中,Mg(OH)2和Fe(OH)2呈胶状物或絮状物沉淀;而Mg
铜及其化合物之间的转化如图所示 运用初中所学的知识分析 在一定条件下不能一步实现的是( )A.①B
铜及其化合物之间的转化如图所示,运用初中所学的知识分析,在一定条件下不能一步实现的是( )A.①B.②C.③D.④












