有A B C D四种钠的化合物 根据下列反应式判断A B C D的化学式。AB+CO2+H2O ;D
| 有A、B、C、D四种钠的化合物,根据下列反应式判断A、B、C、D的化学式。 A 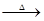 B+CO2+H2O ;D+CO2 B+CO2+H2O ;D+CO2 B+O2 ;D+H2O B+O2 ;D+H2O C+O2↑; C+O2↑;B+Ca(OH)2  C+CaCO3↓。 C+CaCO3↓。(1)写出A、B、C、D的化学式:A__________,B_________,C__________,D__________。 (2)1mol D 与足量CO2反应生成标准状况下的O2 的体积为_____。 |
参考解答
| (1)NaHCO3 、Na2CO3、NaOH、Na2O2 (2) 11.2L |
| 由于四种物质都含有钠元素,所以根据转化关系可知,A是碳酸氢钠,B是碳酸钠,C是氢氧化钠,D是过氧化钠。过氧化钠和CO2反应的方程式为2Na2O2+2CO2=2Na2CO3+O2,所以1mol过氧化钠生成0.5mol氧气,在标准状况下的体积是0.5mol×22.4L/mol=11.2L。 |
相似问题
关于钠的叙述中 正确的是 A.钠在空气中燃烧生成过氧化钠B.钠是银白色金属 硬度很大C.钠投入乙醇中
关于钠的叙述中,正确的是 A.钠在空气中燃烧生成过氧化钠B.钠是银白色金属,硬度很大C.钠投入乙醇中,会浮在液面D.钠的保存要注意防水、防空气
(8分)加热10.0克碳酸钠和碳酸氢钠混合物质质量不再变化 剩余固体的质量为8.45克 求混合物中
(8分)加热10 0克碳酸钠和碳酸氢钠混合物质质量不再变化,剩余固体的质量为8 45克,求混合物中碳酸钠的质量分数。
以海水中常见物质NaCl为原料可以发展很多种工业 (1)写出电解饱和食盐水的化学方程式_______
以海水中常见物质NaCl为原料可以发展很多种工业,(1)写出电解饱和食盐水的化学方程式______________________。(2)以氯碱工业中的某些物质为原料制取
把一定量的铁粉放入氯化铁溶液中 充分反应后所得溶液中Fe3+和Fe2+的浓度恰好相等 则反应的铁和未
把一定量的铁粉放入氯化铁溶液中,充分反应后所得溶液中Fe3+和Fe2+的浓度恰好相等,则反应的铁和未反应的Fe3+的物质的量之比为A.1︰3B.1︰2C.1︰1D.3︰1
在空气中长时间放置少量金属钠 最终的产物是( )(A)NaOH (B)Na2O
在空气中长时间放置少量金属钠,最终的产物是()(A)NaOH(B)Na2O(C)Na2CO3(D)Na2O2












