称取纯Na2CO3 0.53g 用未知浓度的盐酸滴定 恰好完全反应时 用去10mL盐酸。取此盐酸20
| 称取纯Na2CO3 0.53g,用未知浓度的盐酸滴定,恰好完全反应时,用去10mL盐酸。取此盐酸20mL(稀释到200mL)做如下实验:称取工业烧碱6.25g加水溶解至1L,用上述稀释后的盐酸滴定,达到终点时,稀盐酸和烧碱溶液的体积比为3:2,求工业烧碱的纯度。 |
参考解答
| 解:设盐酸的浓度为c 2× 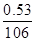 =c×10×10-3 =c×10×10-3c=1mol/L (2分) 则稀盐酸浓度为c’=0.1mol/L 设烧碱纯度为x 0.1×3= 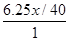 ×2 ×2x=96% (5分) 答:工业烧碱的纯度为96% |
试题分析:设盐酸的浓度为c 2× 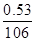 =c×10×10-3 =c×10×10-3c=1mol/L (2分) 则稀盐酸浓度为c’=0.1mol/L 设烧碱纯度为x 0.1×3= 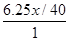 ×2 ×2x=96% (5分) 答:工业烧碱的纯度为96% 点评:解答关于化学计算的题目,学生一定要抓住实质,此题便不难解决。 |
相似问题
关于钠的叙述中 正确的是A.钠是银白色金属 硬度很大B.将金属钠放在坩埚里用酒精灯加热 生成淡黄色固
关于钠的叙述中,正确的是A.钠是银白色金属,硬度很大B.将金属钠放在坩埚里用酒精灯加热,生成淡黄色固体氧化钠C.金属钠在空气中燃烧,产生黄色火焰,
下列除去碳酸钠固体中少量碳酸氢钠的方法正确的是A.加入盐酸B.加入氢氧化钙C.加入氯化钡D.加热
下列除去碳酸钠固体中少量碳酸氢钠的方法正确的是A.加入盐酸B.加入氢氧化钙C.加入氯化钡D.加热
2.3g钠投入100g水中 下列叙述述错误的是A.钠浮在水面 熔化成银色光亮的小球B.钠贮存在煤油中
2 3g钠投入100g水中,下列叙述述错误的是A.钠浮在水面,熔化成银色光亮的小球B.钠贮存在煤油中C.所得溶液的质量分数为2 25﹪D.反应中转移0 1mol电子
工业生产纯碱的工艺流程示意图如下:完成下列填空:(1)粗盐水加入沉淀剂A B除杂质(沉淀剂A来源于石
工业生产纯碱的工艺流程示意图如下:完成下列填空:(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式A.,B (2)实验室提纯
关于Na2CO3 NaHCO3性质的有关叙述不正确的是A.热稳定性:Na2CO3>NaHCO3B.N
关于Na2CO3、NaHCO3性质的有关叙述不正确的是A.热稳定性:Na2CO3>NaHCO3B.NaHCO3能与NaOH溶液反应而Na2CO3则不能C.Na2CO3能转化成NaHCO3,而NaHCO3也












