(11分)(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂 它的氧化性比高锰酸钾更强
| (11分)(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。它是由硝酸铁、氢氧化钠和氯气在一定条件下制得的,同时还生成硝酸钠和氯化钠等。 ①写出制取高铁酸钠的化学方程式: ; ②在制取高铁酸钠的反应中 元素被氧化; ③高铁酸钠之所以有净水作用,除杀菌外,另一个原因是 。 (2)在某化工厂生产中,要用到一种无色、可溶于水的晶体铝铵矾。该晶体是一种复盐,其主要化学成分为十二水合硫酸铝铵。向该复盐的浓溶液中逐滴加入浓氢氧化钠溶液。将发生一系列变化。已知,NH4+与AlO2—在水溶液中不能大量共存,会发生如下反应:NH4++A1O2—+H2O=Al(OH)3↓+ NH3↑ 试回答: ①硫酸铝铵在水溶液中的电离方程式为 ; ②在逐滴加入浓氢氧化钠溶液的过程中,产生的现象有:a溶液中出现白色沉淀;b有刺激性气体逸出;c白色沉淀量逐渐增多;d白色沉淀完全消失;e白色沉淀逐渐减少。 请回答各种现象由先到后出现的顺序是(用序号回答): 。 ③并在下图中画出氢氧化钠的加入体积与沉淀量的关系.  |
参考解答
| (1) ①2Fe(NO3)3+16NaOH+3Cl2=2Na2FeO4 +6NaNO3 +6NaCl + 8 H2O ②铁元素 ③FeO42-被还原为铁离子,铁离子水解生成的氢氧化铁胶体具有很强的吸附性,达到净水的作用。 (2) ①NH4Al(SO4)2= NH4+ + Al3++ 2SO42— ②acbed ③ 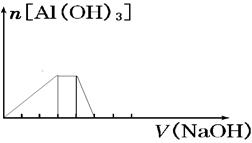 |
| 略 |
相似问题
.欲检验一瓶中装的是稀氨水 现用一沾有浓盐酸的玻棒靠近瓶口 为了使现象明显 可事先往瓶中加入下列哪种
.欲检验一瓶中装的是稀氨水,现用一沾有浓盐酸的玻棒靠近瓶口,为了使现象明显,可事先往瓶中加入下列哪种物质①浓H2SO4 ②固体烧碱 ③固体P2O5 ④生
制取Na2O时 通常采用的方法是:2NaNO2+6Na====4Na2O+N2↑。试说明不用金属钠在
制取Na2O时,通常采用的方法是:2NaNO2+6Na====4Na2O+N2↑。试说明不用金属钠在氧气中燃烧的方法制备Na2O的原因。
(9分)将2.5g碳酸钠 碳酸氢钠和氢氧化钠的固体混合物完全溶解于水 制成稀溶液 然后向该溶液中逐滴
(9分)将2 5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸的体积与产生CO2的
在过氧化钾与水的反应中 其还原产物和氧化产物质量比为( )A.7∶4B.4∶7C.7∶2D.2∶7
在过氧化钾与水的反应中,其还原产物和氧化产物质量比为( )A.7∶4B.4∶7C.7∶2D.2∶7
有关NaHCO3与Na2CO3的说法正确的是A Na2CO3俗称纯碱 所以Na2CO3属于碱B 将石
有关NaHCO3与Na2CO3的说法正确的是A Na2CO3俗称纯碱,所以Na2CO3属于碱B 将石灰水加入到NaHCO3溶液中不产生沉淀C NaHCO3遇到盐酸放出CO2的反应要比Na2












