氯碱厂电解饱和食盐水制取NaOH溶液的工艺流程示意图如下所示 完成下列填空:(1)在电解过程中 与电
氯碱厂电解饱和食盐水制取NaOH溶液的工艺流程示意图如下所示,完成下列填空: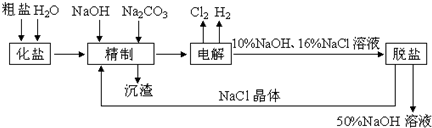 (1)在电解过程中,与电源正极相连的电极上电极反应为______,与电源负极相连的电极附近,溶液pH______(选填“不变”、“升高”或“下降”). (2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为______. (3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是______. a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2 (4)为了有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为______(选填a、b、c) a.先加NaOH,后加Na2CO3,再加钡试剂 b.先加NaOH,后加钡试剂,再加Na2CO3 c.先加Na2CO3,后加NaOH,再加钡试剂. |
参考解答
| (1)电解食盐水,与正极相连为阳极,生成氯气,该电极反应为2Cl--2e-═Cl2↑,与电源负极相连为阴极,生成氢气和NaOH,生成碱,所以pH升高, 故答案为:2Cl--2e-═Cl2↑;不变; (2)Ca2+、Mg2+等杂质与碳酸钠、NaOH反应转化为沉淀,离子反应分别为Ca2++CO32-═CaCO3↓、Mg2++2OH-═Mg(OH)2↓, 故答案为:Ca2++CO32-═CaCO3↓、Mg2++2OH-═Mg(OH)2↓; (3)添加钡试剂除去SO42-,注意不能引入新的杂质,选Ba(NO3)2会引入杂质硝酸根离子,所以选ac,故答案为:ac; (4)有效除去Ca2+、Mg2+、SO42-,应注意碳酸钠在钡试剂之后,是为除去过量的钡离子,显然只有选项b符合,故答案为:b. |
相似问题
如图所示 a b c d均为石墨电极 通电一段时间后 各电极上的生成物的物质的量之比依次为4:1:2
如图所示,a、b、c、d均为石墨电极,通电一段时间后,各电极上的生成物的物质的量之比依次为4:1:2:2,则甲、乙两池中的电解质分别是( )A.AgNO3
下图两个装置中 溶液体积均为200mL 开始时 电解质溶液的浓度均为0.1mol/L 工作一段时间后
下图两个装置中,溶液体积均为200mL,开始时,电解质溶液的浓度均为0.1mol L,工作一段时间后,测得导线上都通过了0.02mol e-,若不考虑溶液体积的变
下列描述中 不符合生产实际的是( )A.合成氨工业中 N2和H2的最佳配比应为物质的量之比1:3B
下列描述中,不符合生产实际的是( )A.合成氨工业中,N2和H2的最佳配比应为物质的量之比1:3B.电解法精炼粗铜,用纯铜作阴极C.工业上电解饱和食盐
某溶液中含有两种溶质NaCl和H2SO4 它们的物质的量之比为3:1.用石墨作电极电解该混合溶液时
某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3:1.用石墨作电极电解该混合溶液时,根据电极产物,可明显分为三个阶段.下列叙述正确的是(
如图所示 A池用石墨电极电解氢氧化钠溶液 B池精炼粗铜 一段时间后停止通电 A池D极产生的气体在标准
如图所示,A池用石墨电极电解氢氧化钠溶液,B池精炼粗铜,一段时间后停止通电,A池D极产生的气体在标准状况下为2 24L.下列说法正确的是( )A.A池为












