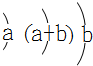有关元素X Y Z W的信息如下:元素有关信息X原子半径为0.074nm 其氢化物的结构模型可表示为
有关元素X、Y、Z、W的信息如下:
(1)Z在元素周期表中的位置是______. (2)Y与W相比,非金属性较强的是______(填元素符号),下列事实能证明这一结论的是______(填字母). a.W元素氢化物的稳定性大于Y元素氢化物的稳定性 b.W元素氢化物水溶液的酸性强于Y元素氢化物水溶液的酸性 c. W元素的单质能与Y元素的氢化物反应,置换出Y单质 d. W的最高价含氧酸比Y的最高价含氧酸的酸性强 (3)Z元素和X元素可形成离子ZX42-,含该离子的盐是优良的绿色消毒剂和无机絮凝剂. ZX42-具有强氧化性,能杀菌消毒,还原产物是Z3+,含该离子的盐用作絮凝剂的原因是(用离子方程式和简要的文字说明)______. |
参考解答
| (1)Z为Fe元素,原子序数为26,位于周期表第四周期、Ⅷ族,故答案为:第四周期、Ⅷ族; (2)同周期元素从左到右元素的非金属性逐渐增强,则非金属性较强的元素为Cl,比较元素的非金属性,可根据 氢化物的稳定性、最高价含氧酸的酸性以及单质之间的置换反应,但不能根据氢化物的酸性,如硫化氢的酸性比水强,但非金属性S的比O弱,不能作为判断的依据, 故答案为:Cl;acd; (3)FeO42-具有强氧化性,可为还原生成Fe3+,Fe3+易水解生成Fe(OH)3胶体,具有较强的吸附性,可起到净水作用, 水解反应的离子方程式为Fe3++3H2O?Fe(OH)3(胶体)+3H+, 故答案为:FeO42-的还原产物为Fe3+,能发生水解反应,Fe3++3H2O?Fe(OH)3(胶体)+3H+,生成的氢氧化铁胶体有吸附作用,起到净水作用. |
相似问题
X Y Z W是原子序数依次增大的四种短周期元素.X与W可形成正四面体型的共价化合物 Y的次外层电子
X、Y、Z、W是原子序数依次增大的四种短周期元素.X与W可形成正四面体型的共价化合物,Y的次外层电子数等于其最外层和最内层电子数之和的2倍,Y、Z的最外
在人体所需的十多种微量元素中 有一种称为“生命元素”的R元素 对延长人类寿命起着重要的作用.已知R元
在人体所需的十多种微量元素中,有一种称为“生命元素”的R元素,对延长人类寿命起着重要的作用.已知R元素的原子有四个电子层,其最高价氧化物分子式为R
三种最外层电子数相同的非金属元素X Y Z 其氢化物的化学式分别是HX HY HZ 经测定HX在50
三种最外层电子数相同的非金属元素X、Y、Z,其氢化物的化学式分别是HX、HY、HZ,经测定HX在500℃时分解1%,HY在150℃时分解10%,HZ在1000℃时仍未分解.
X Y Z W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y W形成X2Y X2Y2
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子
A B C D E五种短周期元素 核电荷数依次增加 其中B的最外层电子数是内层电子总数的2倍 它们可
A、B、C、D、E五种短周期元素,核电荷数依次增加,其中B的最外层电子数是内层电子总数的2倍,它们可形成含有非极性键的B2A2、A2C2、D2C2的化合物;E的单