(10分)磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料 它们的结构相似 右下图为磷化硼晶体
(10分)磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,右下图为磷化硼晶体结构中最小的重复结构单元。磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr。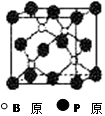 回答下列问题: (1)上述反应物中含有一种元素,其基态原子具有八种不同能量电子,写出其基态原子的价电子轨道表示式 。 (2)BP中每个B或P原子均形成4个共价键,其中有一个配位键,提供空轨道是 原子。 (3)磷化硼的晶体类型是 ,B原子的杂化方式是 ,每生成1molBP,共形成 molB-P键。 (4)已知BBr3+PBr3+3H2=BP+6HBr反应中,P元素被还原,判断电负性:P B (填“>”、“<”) (5)BBr3分子中,B原子采取 杂化,键角为 (6)氮化硼晶体的熔点要比磷化硼晶体高,其原因是 。 |
参考解答
(10分)(1)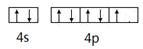 (1分)(2)B (1分) (1分)(2)B (1分)(3)原子晶体;sp3 , 4 (各1分,共3分)(4)> (1分) (5)sp2,非极性 (各1分,共2分) (6)磷原子的半径比氮原子大,N—P共价键键长比B—P小,键能大 (2分) |
试题分析:(1)基态原子具有八种不同能量电子,说明核外有8个能级,所以是溴元素,其基态原子的价电子轨道表示式是 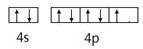 。 。(2)由于B原子的最外层电子数是3个,所以P原子提供孤对电子,B原子提供空轨道。 (3)由于BP属于耐磨涂料,所以形成的晶体应该是原子晶体。B原子形成4个共价键,所以每生成1molBP,共形成4molB-P键,其中B原子的杂化方式是sp3杂化。 (4)P元素被还原,说明P元素的非金属性强于B元素的,所以电负性是P元素的大。 (5)由于BBr3分子中,B原子没有孤对电子对数,所以是平面三角形结构,B原子采取sp2杂化杂化,键角为120°。 (6)由于二者形成的晶体都是原子晶体,而磷原子的半径比氮原子大,N—P共价键键长比B—P小,键能大,因此氮化硼晶体的熔点要比磷化硼晶体高。 点评:该题的关键是根据物质的性质准确判断出晶体类型,而在判断杂化类型时,需要首先判断分子的结构。 |
相似问题
某元素X原子的质量数为A 它的阴离子Xn-核外有x个电子 w克这种元素的原子核内中子为 [
某元素X原子的质量数为A,它的阴离子Xn-核外有x个电子,w克这种元素的原子核内中子为 [ ]A B C D
主族元素A B形成的阴离子如图所示 其中A B原子最外层都已达到8电子稳定结构 则下列关于该离子的叙
主族元素A、B形成的阴离子如图所示,其中A、B原子最外层都已达到8电子稳定结构,则下列关于该离子的叙述肯定错误的是A.n=2 B.A是第ⅡA族元素C.A为-2
2009年3月1日16时13分 中国嫦娥一号卫星成功撞月 标志着我国实施绕月探测的阶段性胜利。其任务
2009年3月1日16时13分,中国嫦娥一号卫星成功撞月,标志着我国实施绕月探测的阶段性胜利。其任务之一是探测月球土壤厚度、探明氦-3 (3He)储量。下列
下列叙述正确的是A.非金属原子间以共价键结合的物质一定是共价化合物B.含有共价键的化合物一定是共价化
下列叙述正确的是A.非金属原子间以共价键结合的物质一定是共价化合物B.含有共价键的化合物一定是共价化合物C.凡是能电离出离子的化合物一定是离子化合
(1)甲醛易溶于水的原因是_____________________________________
(1)甲醛易溶于水的原因是_______________________________________。(2)沸点:甲醇_______甲醛(填“>”或“<”);原因:_________________________。












