硼镁泥是一种工业废料 主要成份是MgO(占40%) 还有CaO MnO Fe2O3 FeO Al2O
硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的工艺流程如下: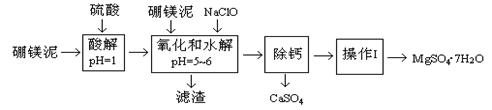 已知:NaClO与Mn2+反应产生MnO2沉淀。
根据题意回答下列问题: (1)实验中需用1.00mol/L的硫酸80.0mL,若用98%的浓硫酸配制,除量筒、玻璃棒、胶头滴管外,还需要的玻璃仪器有 、 。 (2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3外,还有 、 。 (3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式: 。 在调节pH=5~6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为: 。 (4)为了检验滤液中Fe3+是否被除尽,可选用的试剂是 。 A.KSCN溶液 B.淀粉KI溶液 C.H2O2 D.KMnO4稀溶液 (5)已知MgSO4、CaSO4的溶解度如下表:
(6)如果测得提供的硼镁泥的质量为100.0g,得到的MgSO4·7H2O196.8g,则MgSO4·7H2O的产率为 (相对分子质量:MgSO4·7H2O-246 MgO-40)。 |
参考解答
| (1)烧杯、100mL容量瓶(2分) (2)MnO2,SiO2(2分) (3)Mn2++ClO-+H2O=MnO2↓+2H++Cl-(3分) 2Fe2++ClO-+2H+=2Fe3++Cl-+H2O(3分)(4)A(2分) (5)蒸发浓缩,趁热过滤(2分) (6)80.0%(2分,写80%也给分) |
试题分析:(1)由于实验室没有80ml容量瓶,所以要配制1.00mol/L的硫酸80.0mL,则需要100ml容量瓶。所以若用98%的浓硫酸配制,除量筒、玻璃棒、胶头滴管外,还需要的玻璃仪器有烧杯和100ml容量瓶。 (2)由于NaClO与Mn2+反应产生MnO2沉淀,又因为于二氧化锰和二氧化硅都不与稀硫酸反应,所以在滤渣中存在,因此滤纸中还有MnO2,SiO2。 (3)由于NaClO与Mn2+反应产生MnO2沉淀,在反应中氯元素的化合价从+1价降低到-1价,得到2个电子。Mn元素的化合价从+2价升高到+4价,失去2个电子,因此氧化剂与还原剂的物质的量之比是1:1,则NaClO与Mn2+反应产生MnO2沉淀的离子方程式为Mn2++ClO-+H2O=MnO2↓+2H++Cl-;由于溶液中有亚铁离子,能够被次氯酸钠氧化成铁离子,反应的离子方程式为:2Fe2++ClO-+2H+=2Fe3++Cl-+H2O。 (4)铁离子能和KSCN溶液反应使溶液显红色,所以可以向溶液中加入硫氰化钾溶液检验溶液中是否存在三价铁离子,方法为:取少量滤液,向其中加入硫氰化钾溶液,如果溶液不变红色,说明滤液中不含Fe3+;如果溶液变红色,说明滤液中含Fe3+,A正确;由于溶液中含有次氯酸钠,能氧化碘化钾,所以不能使用碘化钾,B不正确;双氧水和酸性高锰酸钾溶液均具有强氧化性,不能检验铁离子,CD不正确,答案选A。 (5)由于温度对硫酸镁、硫酸钙的溶解度影响不同,温度越高,硫酸钙溶解度越小,所以要将MgSO4和CaSO4混合溶液中的CaSO4除去可以采用蒸发浓缩,趁热过滤方法除去硫酸钙;而操作“I”是将滤液继续蒸发浓缩,冷却结晶,再经过过滤,便得到了MgSO4?7H2O。 (6)100g硼镁泥中氧化镁的物质的量= 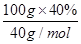 =1mol,根据镁原子守恒,生成MgSO4?7H2O的物质的量为1mol,质量为246g/mol×1mol=246g,所以MgSO4?7H2O的产率= =1mol,根据镁原子守恒,生成MgSO4?7H2O的物质的量为1mol,质量为246g/mol×1mol=246g,所以MgSO4?7H2O的产率=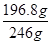 ×100%=80.0%。 ×100%=80.0%。 |
相似问题
下列实验能达到目的的是A.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中 检验气体中含有乙烯B
下列实验能达到目的的是A.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中,检验气体中含有乙烯B.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪
甲 乙 丙 丁四种易溶于水的物质 分别由Na+ Ba2+ Al3+ H+ OH- Cl- HC
甲、 乙、 丙、 丁四种易溶于水的物质,分别由Na+、Ba2+、Al3+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成,已知:①0 1
现从锌制品加工企业回收的废渣(含有ZnO FeO Fe2O3 CuO Al2O3等杂质)来制取氧化锌
现从锌制品加工企业回收的废渣(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质)来制取氧化锌,流程如下:有关氢氧化物完全沉淀的pH见下表:沉淀物Al(OH)3Fe(OH
下列实验操作中正确的是( )A.蒸馏操作时 应向蒸馏烧瓶中加入几块沸石 以防止暴沸B.蒸发操作时 应
下列实验操作中正确的是()A.蒸馏操作时,应向蒸馏烧瓶中加入几块沸石,以防止暴沸B.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热C.蒸发
下列离子检验的方法正确的是A.某溶液生成白色沉淀 说明原溶液中有Cl-B.某溶液生成白色沉淀 说明原
下列离子检验的方法正确的是A.某溶液生成白色沉淀,说明原溶液中有Cl-B.某溶液生成白色沉淀,说明原溶液中有SO42-C.某溶液生成红褐色沉淀,说明原溶












