(10分)某化学反应的反应物和产物如下:KMnO4 + KI+ H2SO4→ MnSO4 + I2
| (10分)某化学反应的反应物和产物如下: KMnO4 + KI+ H2SO4→ MnSO4 + I2 + KIO3 + K2SO4 + H2O (1)该反应的氧化剂是 。 (2)如果该反应方程式中I2和KIO3的化学计量数都是5 ①KMnO4的化学计量数是 。 ②在下面的化学式上标出电子转移的方向和数目 KMnO4 + KI + H2SO4 → (3)如果没有对该方程式中的某些化学计量数作限定,可能的配平化学计量数有许多组。原因是 。 |
参考解答
(1)KMnO4 (2)① 8 ② 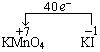 (3)该反应式含两种氧化产物,两者的比例和氧化剂的用量都可以发生变化 解析:KMnO4中Mn元素的化合价降低,KMnO4是氧化剂。配平的化学方程式为: 8KMnO4 + 15KI+ H2SO4→ 8MnSO4 + 5I2 + 5KIO3 + 9K2SO4 + 17H2O 转移的电子总数为40,故KMnO4的化学计量数是8, |
| 略 |
相似问题
根据下列反应:①?Cu+2FeCl3═2FeCl2+CuCl2?②2FeCl2+Cl2═2FeCl3
根据下列反应:①?Cu+2FeCl3═2FeCl2+CuCl2?②2FeCl2+Cl2═2FeCl3?③MnO2+4HCl(浓)△ MnCl2+Cl2↑+2H2O判断以下各组物质的氧化性由强到弱顺序正确的是
根据下列反应判断有关的物质氧化性由强到弱的顺序是( )H2SO3+I2+H2O=2HI+H2SO4
根据下列反应判断有关的物质氧化性由强到弱的顺序是( )H2SO3+I2+H2O=2HI+H2SO42FeCl3+2HI=2FeCl2+2HCl+I23FeCl2+4HNO3=2FeCl3+NO↑+2H2O+Fe(NO3)3
由amolFe+bmolFe2O3组成的混和物 用足量的盐酸溶解。随着a/b的不同 反应产物各不相同
由amolFe+bmolFe2O3组成的混和物,用足量的盐酸溶解。随着a b的不同,反应产物各不相同。按照a b的不同比值,结合有关氧化还原的反应竞争顺序,填写下列
根据下列化学方程式 判断有关物质的还原性强弱顺序正确的是①I2+SO2+2H2O=H2SO4+2HI
根据下列化学方程式,判断有关物质的还原性强弱顺序正确的是①I2+SO2+2H2O=H2SO4+2HI;②2FeCl2+Cl2=2FeCl3;③2FeCl3+2HI=2FeCl2+2HCl+I2A.I-
氯和硫都是重要的非金属元素。下列叙述不能说明氯的非金属性比硫强的是A.氯化氢的沸点比硫化氢的沸点高B
氯和硫都是重要的非金属元素。下列叙述不能说明氯的非金属性比硫强的是A.氯化氢的沸点比硫化氢的沸点高B.与氢气反应时,氯气比硫更容易C.氯气可以从氢












