A B C D E是五种中学常见的单质 已知A B C D在常温下均为气体.E是地壳中含量居第二位的
| A、B、C、D、E是五种中学常见的单质,已知A、B、C、D在常温下均为气体.E是地壳中含量居第二位的金属.D可分别跟A、B、C在一定的条件下化合,生成X、Y、Z;Y、Z与Ne的电子数相等,A是第三周期的元素.有关的转化关系如下图所示(反应条件均已略去): (1)A的化学式为______,B的化学式为______,C的电子式为______. (2)Z和W在催化剂和加热的条件下反应生成C和Y,这是一个很有意义的反应,可以消除W对环境的污染,该反应的化学方程式为______. (3)将N溶液滴入G的溶液中会产生W,写出上述变化的离子反应方程式:______. (4)Z与N恰好反应后产物溶解在水中,所得溶液的pH(填“大于”、“小于”或“等于”)______7,用离子反应方程式表示其原因为______. 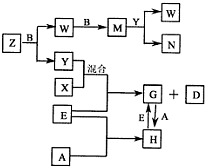 |
参考解答
| A、B、C、D、E是五种中学常见的单质,已知A、B、C、D在常温下均为气体.E是地壳中含量居第二位的金属,则E为铁;Y、Z与Ne的电子数相等,则Y、Z为10电子微粒,再由框图中G与H的转化可知,A是第三周期的元素,A在常温下为气体,则A为氯气,H为氯化铁,G为氯化亚铁;再由转化中X与Y混合与铁反应,则D为氢气,X为氯化氢,Y为水,即B为氧气;由Z和B→W,W和B→M,M和Y反应生成W和N,则Z为氨气,即C为氮气,W为NO,M为NO2,N为硝酸; (1)因A为氯气,其化学式为Cl2,B为氧气,其化学式为O2,C为氮气,其电子式为 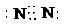 ,故答案为:Cl2;O2; 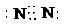 ; (2)Z和W在催化剂和加热的条件下反应生成C和Y,即氨气和NO反应生成氮气和水,其反应为6NO+4NH3 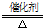 5N2+6H2O, 故答案为:6NO+4NH3 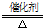 5N2+6H2O; (3)将N溶液滴入G的溶液中会产生W,即硝酸滴到氯化亚铁溶液中发生氧化还原反应生成NO,离子反应为4H++NO3-+3Fe2+═NO↑+2H2O+3Fe3+, 故答案为:4H++NO3-+3Fe2+═NO↑+2H2O+3Fe3+; (4)Z与N恰好反应后产物溶解在水中所得溶液为硝酸铵溶液,由铵根离子的水解反应NH4++H2O  NH3?H2O+H+可知该溶液显酸性,溶液的pH小于7, 故答案为:小于;NH4++H2O  NH3?H2O+H+. |
相似问题
据最新报道 科学家发现了如下反应:O2+PtF6=O2 (PtF6) 已知O2(PtF6)为离子化合
据最新报道,科学家发现了如下反应:O2+PtF6=O2(PtF6),已知O2(PtF6)为离子化合物,其中Pt为+5价,对于此反应,下列说法正确的是( )A.O2(PtF6
下列叙述正确的是( )A.元素的单质一定由氧化或还原该元素的化合物制得B.在化学反应中 得电子越多
下列叙述正确的是( )A.元素的单质一定由氧化或还原该元素的化合物制得B.在化学反应中,得电子越多的氧化剂,其氧化性就越强C.阳离子只能得到电子
阿波罗宇宙飞船以N2H4(联氨)和N2O4为动力源 反应温度达2700℃ 反应方程式为:2N2H4+
阿波罗宇宙飞船以N2H4(联氨)和N2O4为动力源,反应温度达2700℃,反应方程式为:2N2H4+N2O4=3N2+4H2O,关于该反应的说明中正确的是( )A.属于置换
实验室中 通常以草酸钠(Na2C2O4)为标准液 通过氧化还原滴定来测定高锰酸钾溶液的浓度 其反应的
实验室中,通常以草酸钠(Na2C2O4)为标准液,通过氧化还原滴定来测定高锰酸钾溶液的浓度,其反应的化学方程式为:C2O42-+MnO4-+H+-Mn2++CO2↑+H2O(未配
工业甲醇的质量分数可以用下列方法测定:①在稀H2SO4中甲醇被Cr2O72-氧化成CO2和H2O 反
工业甲醇的质量分数可以用下列方法测定:①在稀H2SO4中甲醇被Cr2O72-氧化成CO2和H2O,反应式为:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O;②过量的Cr2O72-可












