稀硝酸和足量的铁反应的化学方程式如下:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O(1
| 稀硝酸和足量的铁反应的化学方程式如下:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O (1)该氧化还原反应的氧化剂是______,氧化产物是______.用双线桥法在化学方程式中表示出电子转移的方向和数目为:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O (2)此反应的离子方程为______. (3)若生成标准状况下11.2LNO气体,计算参加反应的铁的质量以及反应中被还原的HNO3的物质的量. |
参考解答
(1)该反应中,硝酸得电子作氧化剂,铁失电子作还原剂,铁对应的产物硝酸亚铁是氧化产物,该反应中铁失去电子数=3(2-0)=6,硝酸得电子数=2(5-2)=6,所以用双线桥法在化学方程式中表示出电子转移的方向和数目为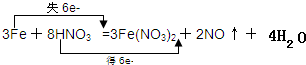 , 故答案为:HNO3;Fe(NO3)2; 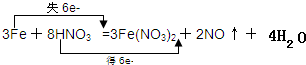 ; (2)该反应的离子方程式为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故答案为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O; (3)设参加反应的铁的质量为m, 被还原的HNO3的物质的量为n 由 3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O 3×56g 2mol(被还原) 2×22.4L m n 11.2L 得 m=
n=
答:参加反应铁的质量是42g,被还原的硝酸的物质的量是0.5mol. |
相似问题
下列变化中 需要加入还原剂的是( )A.2Cl-→Cl2B.Fe2+→Fe3+C.Cu2+→CuD
下列变化中,需要加入还原剂的是( )A.2Cl-→Cl2B.Fe2+→Fe3+C.Cu2+→CuD.MnO4-→MnO2
下面是有关厨房中的常见操作或者常见现象 其中不涉及氧化还原反应的是( )A.烧菜用过的铁锅 经放置
下面是有关厨房中的常见操作或者常见现象,其中不涉及氧化还原反应的是( )A.烧菜用过的铁锅,经放置常出现红棕色斑迹B.用煤气灶燃烧天然气为炒菜
下列物质放置在空气中 因发生氧化还原反应而变质的是( )A.Na2O2B.Na2OC.NaOHD.
下列物质放置在空气中,因发生氧化还原反应而变质的是( )A.Na2O2B.Na2OC.NaOHD.NaHCO3
已知铜在常温下能被稀硝酸溶解 其反应的化学方程式如下3Cu+8HNO3═3Cu(NO3)2+2NO↑
已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O(1)用双线桥法分析上述反应(只需标出电子得失的方向和数目
化合物A是尿路结石的主要成分 属于结晶水合物 可用X?H2O表示.在一定条件下有如图(1)所示的转化
化合物A是尿路结石的主要成分,属于结晶水合物,可用X?H2O表示.在一定条件下有如图(1)所示的转化关系:已知:①经分析,图(1)中的各字母代表的物质












