(4分)配平氧化还原反应方程式。(1) NH3+ NO2— N2+
| (4分)配平氧化还原反应方程式。 (1) NH3+ NO2— N2+ H2O (2) 氧化产物与还原产物的质量比为 。 |
参考解答
| (4分)(1)8 6 14 12 (2)4:3 |
| 本题考查氧化还原反应方程式的配平 (1) 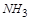 中 中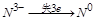 , ,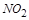 中 中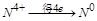 ,得失电子数的最小公倍数为 ,得失电子数的最小公倍数为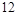 , ,在 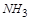 前配系数 前配系数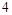 ,在 ,在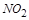 前配系数3,则 前配系数3,则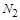 前配系数为 前配系数为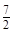 ,再配平 ,再配平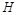 ,在 ,在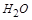 前配 前配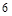 ; ;即 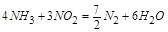 此方程式的两端同乘以 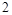 得 得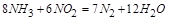 (2) 在反应 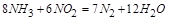 中, 中,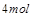 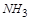 被氧化成 被氧化成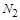 , ,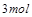 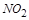 被还原 被还原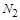 ,产物均为 ,产物均为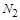 ,因而氧化产物与还原产物的质量比为 ,因而氧化产物与还原产物的质量比为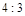 . . |
相似问题
在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中 每摩尔CuSO
在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,每摩尔CuSO4能氧化P的物质的量为( ) A.1 5 molB.2 5 molC.3 5molD.11 5 mol
RO2受热分解为+4和+2价的混合氧化物 +4价的R能氧化浓盐酸生成Cl2 现将1mol RO2加热
RO2受热分解为+4和+2价的混合氧化物,+4价的R能氧化浓盐酸生成Cl2,现将1mol RO2加热分解得到O2,再向残余固体中加入过量的浓盐酸得到Cl2,所得 O2和Cl2
在水溶液中 YO3n-和S2-发生如下反应:YO3n- + 3S2- +6H+ = Y-+ 3S↓+
在水溶液中,YO3n-和S2-发生如下反应:YO3n-+ 3S2- +6H+ = Y-+ 3S↓+ 3H2O,则YO3n-中Y元素的化合价和原子最外层电子数分别为A.+4、6B.+7、7C.+5、7D.+5、5
已知P单质在KOH溶液中的变化是:4P+3KOH+3H2O=3KH2PO2+PH3↑ 下列说法正确的
已知P单质在KOH溶液中的变化是:4P+3KOH+3H2O=3KH2PO2+PH3↑,下列说法正确的是A.产物PH3分子中所有的原子可能共平面 B.该反应中P做还原剂,H2O做氧化
在SO2+2H2S = 2H2O+3S ↓ 反应中 氧化产物与还原产物的物质的量之比为A.2∶1
在SO2+2H2S=2H2O+3S ↓ 反应中,氧化产物与还原产物的物质的量之比为A.2∶1 B.1∶2 C.3∶1D.1∶3












