(18分)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
(18分)以硫 铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下: 铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下: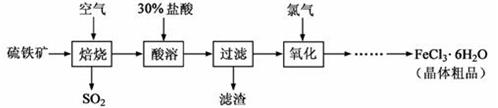 回答下列问题: (1)将煅烧黄铁矿的化学方程式补充完整: +  Fe2O3+ SO2↑;该反应中,FeS2为 剂;SO2为 产物,其常常用于制备硫酸,反应过程中的化学反应方程式为 、 ; Fe2O3+ SO2↑;该反应中,FeS2为 剂;SO2为 产物,其常常用于制备硫酸,反应过程中的化学反应方程式为 、 ;(2)酸溶及后续过程中均需保持盐酸过量,其目的是 、 ; (3)通氯气氧化后时,发生的主要反应的离子方程式为 ; (4)该过程产生的污染空气的气体有三种,尾气均可用强碱溶液吸收,这些反应的离子方程式为 ;。 (5)从FeCl3溶液中得到FeCl3.6H2O晶体的操作为 。 |
参考解答
(1) 4FeS2+11O2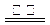 2Fe2O3+8SO2 ↑(2分) 2Fe2O3+8SO2 ↑(2分) 还原剂 既是氧化产物,又是还原产物 2SO2(g)+O2(g)  2SO3(g) SO3+H2O=H2SO4 2SO3(g) SO3+H2O=H2SO4(2)提高铁元素的浸出率 抑制Fe3+水解 (3)Cl2+2Fe2+=2Cl-+2Fe3+ (4) Cl2 +OH-=Cl-+ClO-+H2O H++OH-=H2O SO2+2OH-=SO32- +H2O SO2+OH-=HSO3- (5)在HCl的氛围中,加热浓缩,冷却结晶,过滤(4分) |
| 略 |
相似问题
已知M2O7x一+3S 2一+14H+ ====2M3++3S↓+7H2O 则M2O7x一中的M的化
已知M2O7x一+3S 2一+14H+ ====2M3++3S↓+7H2O,则M2O7x一中的M的化合价为A.+2B.+3 C.+4D.+6
为监测空气中汞蒸气是否超标 通过悬挂涂有CuI(白色)的滤纸 根据滤纸是否变色(亮黄色至暗红色)及变
为监测空气中汞蒸气是否超标,通过悬挂涂有CuI(白色)的滤纸,根据滤纸是否变色(亮黄色至暗红色)及变色所需时间来判断空气中的汞的含量。发生的化学反
依据氧化还原反应:2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)设计的原电池如图所
依据氧化还原反应:2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)设计的原电池如图所示。下列叙述正确的是A.Y为CuSO4溶液B.正极反应为Cu-2e-= Cu2+C.在外
有相同条件下的三个反应:①2A—+B2==2B—+A2 ②2C—+A2==2A—+C
有相同条件下的三个反应:①2A—+B2==2B—+A2 ②2C—+A2==2A—+C2 ③2B—+D2==2D—+B2,由此得出,下列判断不正确的是A.2C—+B2==2B—+C2该反应可以进
(9分)(1)某一反应体系中的物质有:HCl SnCl2 H2SnCl6 As H3AsO3 H2O
(9分)(1)某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O,已知:HCl是反应物之一。①写出配平的该反应的化学方程式:______________












