【物质结构与性质】某配位化合物为深蓝色晶体 由原子序数依次增大的A B C D E五种元素组成 其原
| 【物质结构与性质】 某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素 组成,其原子个数比为l4:4:5:1:1。其中C、D元素同主族且原子序数D为C的 二倍,E元素的外围电子排布为(n-1)dn+6nsl,回答下列问题。 (1)元素B、C、D的第一电离能的由大到小排列顺序为 。(用元素符号表示) (2)D元素原子的最外层电子排布图为 。 (3)该配位化合物的化学式为______,配体的中心原子的杂化方式为 。 (4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,两种化合物可任意比互溶,解释其主要原因为 。 (5)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为 ,分子中含有 个σ键, 个π键。 (6)A元素与E元素可形成一种红色化合物,其晶体结构单元如图。则该化合物的化学式为 。该化合物可在氯气中燃烧,生成一种棕黄色固体和一种气体,写出该反应的化学方程式 。 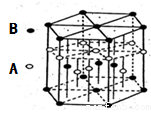 |
参考解答
| (1)N>O>S (2) 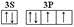 (3)[Cu(NH3)4SO4?H2O。 sp3杂化 (4)H2O与H2O2之间形成氢键 (5)H-N=N-H;3;1 (6)CuH 2CuH+3Cl2  2CuCl2+2HCl 2CuCl2+2HCl |
| 某配位化合物为深蓝色晶体,由原子序数由小到大的A、B、C、D、E五种元素构成,其原子个数比为14:4:5:1:1,其中C、D元素同主族且原子序数D为C的二倍,则C为O元素、D为S元素;E元素的外围电子排布为(n-l)dn+6nsl,则n+6=10,故n=4,故其外围电子排布为3d104sl,则E为Cu;故该深蓝色晶体应含有[Cu(NH3)42+、SO42-,结合原子序数可知A为H、B为N,由原子数目之比,可知该配合物含有1个结晶水,故其化学式为:[Cu(NH3)4SO4?H2O。 (1)同主族自上而下第一电离能减小,故O元素第一电离能大于S元素,O与N元素同周期,N元素原子2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能大于O元素,故第一电离能由大到小的排列顺序为:N>O>S。 (2)D为S元素,其原子的最外层电子排布图为 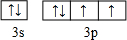 。 。(3)由上述分析可知,该配位化合物的化学式为:[Cu(NH3)4SO4?H2O,配体为NH3,N原子价层电子对数=3+(5?1×3)/2=4,N原子采取sp3杂化。 (4)O元素可与H元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,则为H2O、H2O2,两种化合物可任意比互溶,其主要原因为:H2O与H2O2分子之间存在氢键。 (5)H元素与N元素可形成分子式为N2H2的化合物,该化合物的分子具有平面结构,N原子之间形成N=N双键,N原子与H原子之间形成N-H键,其结构式为H-N=N-H,分子中含有3个σ键,1个π键。 (6)H元素与Cu元素可形成一种红色化合物,由晶体结构单元可知,4个H原子位于内部,6个H原子位于棱上,晶胞中H原子数目=4+6×1/3=6,3个Cu原子为内部,2个位于面心、12个位于顶点,故晶胞中Cu原子数目=3+2×1/2+12×1/6=6,故该化合物的化学式为CuH,该化合物可在氯气中燃烧,生成一种棕黄色固体和一种气体,应生成CuCl2、HCl,反应方程式为: 2CuH+3Cl2  2CuCl2+2HCl。 2CuCl2+2HCl。 |
相似问题
短周期元素X Y Z W在周期表中相对位置如下图所示 Y元素在地壳中的含量最高。下列说法正确的是A.
短周期元素X、Y、Z、W在周期表中相对位置如下图所示,Y元素在地壳中的含量最高。下列说法正确的是A.原子半径:Z<Y<WB.最简单气态氢化物的热稳定性:Y<W
(14分)Ⅰ(1)过渡金属元素有很多不同于主族元素的性质 如能形成多种配合物 如:Fe(CO)x [
(14分)Ⅰ(1)过渡金属元素有很多不同于主族元素的性质,如能形成多种配合物,如:Fe(CO)x、[Fe(H2NCONH2)6] (NO3)3 [三硝酸六尿素合铁(Ⅲ)]、[Cu(NH
下列A B两种元素的原子序数 其中可以组成AB2型离子化合物的是A.6和8 B.19和
下列A、B两种元素的原子序数,其中可以组成AB2型离子化合物的是A.6和8 B.19和16 C.12和17 D.10和8
简单原子的原子结构可用下图形象地表示 其中?表示质子 ○表示中子:①; ②;③。则下列有关这三种原子
简单原子的原子结构可用下图形象地表示,其中?表示质子,○表示中子:①;②;③。则下列有关这三种原子的叙述中正确的是A.属于不同的元素B.具有相同的
下列性质的递变中 正确的是A.O Na S的原子半径依次增大B.LiOH KOH CsOH的碱性依次
下列性质的递变中,正确的是A.O、Na、S的原子半径依次增大B.LiOH、KOH、CsOH的碱性依次增强C.HF、NH3、SiH4的稳定性依次增强D.HCl、HBr、HI的还原性依次减弱












