现有NaHCO3和Na2CO3·xH2O的混合物 为了测定x值 某同学采用如图所示的装置进行实验(C
现有NaHCO3和Na2CO3·xH2O的混合物,为了测定x值,某同学采用如图所示的装置进行实验(CaCl2、碱石灰均足量)。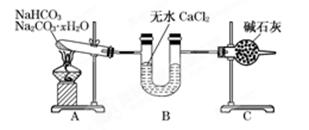 (1)A装置的作用:________________________________________________________________。 (2)B装置的作用是:_______________________________________________________________。 (3)C装置的作用是:_________________________________________________________________。 (4)若在装置A的试管中装入NaHCO3和Na2CO3·xH2O的混合物3.7 g,用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22 g,则x的值为______。 (5)该装置还不是很完善,可能使测定结果偏小,应如何改进________。为什么?___________________________________________________________________________________。 |
参考解答
| (1)加热,使NaHCO3分解,使Na2CO3·H2O失水(2分) (2)吸收反应中生成的水(1分) (3)吸收反应中生成的CO2(2分) (4)10(2分) (5)在C装置后再加一个装有碱石灰的U形管;为了防止空气中的CO2和H2O被C装置的中的碱石灰吸收(2分) |
试题分析:(1)在加热的条件下碳酸氢钠易分解生成碳酸钠、水和CO2,而碳酸钠晶体也易失去结晶水,所以A装置的作用是加热,使NaHCO3分解,使Na2CO3·H2O失水。 (2)无水氯化钙能吸收水蒸气,通过称量反应前后的质量可以得出水蒸气的质量,因此B装置的作用是吸收反应中生成的水。 (3)由于反应中还有CO2生成,而碱石灰可以吸收CO2,因此通过称量反应前后的质量,可以得出CO2的质量,所以C装置的作用是吸收反应中生成的CO2。 (4)用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22 g,这说明反应中生成的水蒸气质量=1.89g,CO2质量=0.22g,物质的量分别是 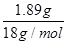 =0.105mol、 =0.105mol、 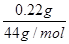 =0.005mol。根据反应的方程式2NaHCO3 =0.005mol。根据反应的方程式2NaHCO3 Na2CO3+H2O+CO2↑可知,该反应中生成的CO2就是0.005mol,则碳酸氢钠的物质的量是0.005mol×2=0.01mol,反应中生成的水是0.005mol。则碳酸钠在反应中失去的水的物质的量=0.105mol-0.005mol=0.100mol。碳酸氢钠的质量=0.01mol×84g/mol=0.84g,则样品中碳酸钠晶体的质量=3.7g-0.84g=2.86g。则 Na2CO3+H2O+CO2↑可知,该反应中生成的CO2就是0.005mol,则碳酸氢钠的物质的量是0.005mol×2=0.01mol,反应中生成的水是0.005mol。则碳酸钠在反应中失去的水的物质的量=0.105mol-0.005mol=0.100mol。碳酸氢钠的质量=0.01mol×84g/mol=0.84g,则样品中碳酸钠晶体的质量=3.7g-0.84g=2.86g。则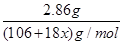 ×x=0.1mol,解得x=10。 ×x=0.1mol,解得x=10。(5)由于空气中也含有CO2和水蒸气,也能被C装置的中碱石灰吸收,从而导致C管增重偏高,因此测量值偏低。所以改进的措施为在C装置后再加一个装有碱石灰的U形管;为了防止空气中的CO2和H2O被C装置的中的碱石灰吸收。 |
相似问题
取16.8g碳酸氢钠固体 加热一段时间后 剩余固体的质量为13.7g。把剩余固体加入到100mL 2
取16 8g碳酸氢钠固体,加热一段时间后,剩余固体的质量为13 7g。把剩余固体加入到100mL 2mol L的稀硫酸中,充分反应后溶液中H+的浓度约为A.3 mol LB.
将过氧化钠和过量的碳酸氢钠在密闭容器中混合充分加热后 最终残留固体物质是A.Na2CO3
将过氧化钠和过量的碳酸氢钠在密闭容器中混合充分加热后,最终残留固体物质是A.Na2CO3 B.Na2O和Na2O2C.Na2O2
将70 g过氧化钠和氧化钠的混合物跟98 g水充分反应后 所得氢氧化钠溶液的质量分数为50%。(1)
将70 g过氧化钠和氧化钠的混合物跟98 g水充分反应后,所得氢氧化钠溶液的质量分数为50%。(1)求原混合物中过氧化钠和氧化钠的质量;(2)产生的气体标况下体积。
(16分)某小组的同学对放置已久的过氧化钠的成份进行探究 请回答下列问题:(1)反应 2Na2O2+
(16分)某小组的同学对放置已久的过氧化钠的成份进行探究,请回答下列问题:(1)反应 2Na2O2+2H2O=4NaOH+O2↑的还原剂是(写化学式);反应2Na2O2
向100mL2mol/L的NaOH溶液中通入一定量的CO2 结晶 得到9.3g白色固体 该白色固体的
向100mL2mol L的NaOH溶液中通入一定量的CO2,结晶,得到9.3g白色固体,该白色固体的组成是A.只含Na2CO3B.只含NaHCO3C.NaOH和Na2CO3的混合物D.Na2CO3和NaHCO3的混合物












