下列可用氢键来解释的是 A.浓的氢氟酸溶液中存在HF和H2FB.SiH4沸点比CH4高C.水和乙醇
下列可用氢键来解释的是
|
参考解答
| A |
| 原子半径小、吸引电子能力强的F、O、N与H原子间易形成氢键,氢键的存在可能会形成缔合物,影响物质的物理性质。B项中,因SiH4的相对分子质量比CH4的相对分子质量大,从而造成前者分子间作用力大,C、D两项均体现物质的化学性质,故只有A项成立。 |
相似问题
(1)在HF H2S NH3 CS2 CH4 N2分子中:①以非极性键结合的非极性分子是______
(1)在HF、H2S、NH3、CS2、CH4、N2分子中:①以非极性键结合的非极性分子是______.②以极性键相结合,具有正四面体结构的非极性分子是______.③以极性
下列说法不正确的是 [ ]A.互为手性异构体的分子互为镜像B.利用手性催化剂合成可主要得到一
下列说法不正确的是 [ ]A.互为手性异构体的分子互为镜像B.利用手性催化剂合成可主要得到一种手性分子C.手性异构体分子组成相同D.手性异构体性质相同
在①HF ②H2S ③BF3 ④CS2 ⑤CCl4 ⑥N2 ⑦SO2分子中:(1)以非极性键结合的非
在①HF、②H2S、③BF3、④CS2、⑤CCl4、⑥N2、⑦SO2分子中:(1)以非极性键结合的非极性分子是______(2)以极性键相结合,具有直线型结构的非极性分子
下列叙述中正确的是[ ]A.2s轨道可以和3p轨道形成sp2杂化轨道 B.烯烃中的碳碳双键由
下列叙述中正确的是[ ]A.2s轨道可以和3p轨道形成sp2杂化轨道 B.烯烃中的碳碳双键由一个σ键和一个π键组成 C.苯分子中存在碳碳双键 D.sp3杂化轨
(三选一)[选修3:物质结构与性质]氢能被视作连接化石能源和可再生能源的重要桥梁。(1)水是制取H2
(三选一)[选修3:物质结构与性质]氢能被视作连接化石能源和可再生能源的重要桥梁。(1)水是制取H2的常见原料,下列有关水的说法正确的是_____________


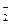 和H2F
和H2F