(14分)下表所示的是第二周期元素中 除Be B Ne三种元素外 其它元素的简单氢化物的沸点;题26
(14分)下表所示的是第二周期元素中,除Be、B、Ne三种元素外,其它元素的简单氢化物的沸点;题26图所示是第三周期元素中,除Ar以外的其它元素的单质的熔点变化关系。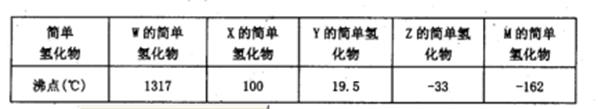 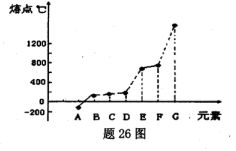 (1)X的简单氢化物属于 分子(填“极性”或“非极性”),G元素的单质在固态时的晶体类型为___ _。 (2)写出W的氢化物的电子式 ______。 (3)A和Z两元素形成的一种化合物分子中各原子最外均达到8电子稳定结构,则该分子的结构式为 。 (4)化合物AY能与水反应生成两种弱酸,其化学方程式为 (5)写出元素F的单质与三氧化二铬反应的化学方程式___ |
参考解答
| (1)极性(2分),原子晶体(2分) (2)Li+[:H-(2分) (3) 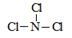 (2分) (4)ClF+H2O=HClO+HF(3分) (2分) (4)ClF+H2O=HClO+HF(3分) (5)2Al+Cr2O3 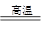 Al2O3+2Cr(3分) Al2O3+2Cr(3分) |
| (1)X的氢化物的沸点是100℃,所以X是水,属于极性分子。G单质的熔点最高,应该是单质硅,属于原子晶体。 (2)W的氢化物最高,应该是离子化合物,而在第二周期中能析出离子晶体的是LiH,电子式为Li+[:H-。 (3)A的熔点最低,应该是氯气。Z的氢化物沸点仅比M的氢化物沸点高,所以Z是氮元素。由于化合物分子中各原子最外均达到8电子稳定结构,所以是NCl3,结构类似于氨气,所以结构式为 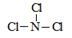 。 。(4)Y是F,非金属性最强,所以ClF和水反应的方程式为ClF+H2O=HClO+HF。 (5)F单质的熔点仅比硅的底,所以F是铝。发生铝热反应,反应式为2Al+Cr2O3 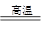 Al2O3+2Cr。 Al2O3+2Cr。 |
相似问题
下列说法中 正确的是A.加热碘化氢气体使之分解只需克服分子间作用力B.氯化氢溶于水能电离出H+ Cl
下列说法中,正确的是A.加热碘化氢气体使之分解只需克服分子间作用力B.氯化氢溶于水能电离出H+、Cl-,所发氯化氢是离子化合物C.氧气与臭氧相互转化属
下列叙述中 错误的是 A.离子化合物中可能含有非极性键B.分子晶体中的分子内不含有离子键C.原子
下列叙述中,错误的是 A.离子化合物中可能含有非极性键B.分子晶体中的分子内不含有离子键C.原子晶体中可能含有非极性键D.分子晶体中的分子内一定有共价键
(12分)A B C D E分别代表五种短周期元素 且原子序数依次增大 已知:B的最外层电子排布是n
(12分)A、B、C、D、E分别代表五种短周期元素,且原子序数依次增大,已知:B的最外层电子排布是nsnnpn+1;C的p能级上未成对的电子比B少一个;D的二价阳
氯化硼的熔点为-107℃ 沸点为12.5℃ 在其分子中键与键之间的夹角为120° 它能水解 有关叙述
氯化硼的熔点为-107℃,沸点为12 5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是A.氯化硼分子呈正三角形,属非极性分子B.氯化
一种称为“摇头丸”的毒品已从国外流入我国 严重损害一些吸毒者的身心健康 司法机关予以坚决查缉和打击。
一种称为“摇头丸”的毒品已从国外流入我国,严重损害一些吸毒者的身心健康,司法机关予以坚决查缉和打击。已知该毒品中氮的质量分数为10 37%,试完成下












