取碳酸钠和氯化钠的混合物10g 投入50g溶质质量分数为9.8%的稀硫酸中 恰好完全反应 假设生成的
| 取碳酸钠和氯化钠的混合物10g,投入50g溶质质量分数为9.8%的稀硫酸中,恰好完全反应,假设生成的气体全部逸出。计算: (1)反应中生成二氧化碳气体的质量; (2)该混合物中碳酸钠的质量分数。 (提示:反应的化学方程式为Na2CO3+H2SO4==Na2SO4+H2O+CO2↑) |
参考解答
| 解:设反应中生成二氧化碳气体的质量为,样品中的碳酸钠的质量为。 Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ 106 98 44 y 50g×9.8% x 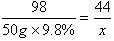 ; ;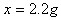 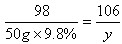 ; ;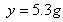 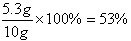 答:生成二氧化碳气体的质量为2.2g,样品中碳酸钠的质量分数为53%。 |
相似问题
化学小组为了测定某铜矿中碱式碳酸铜[Cu2(OH)2CO3]的质量分数.称取该铜矿样品30g于烧杯中
化学小组为了测定某铜矿中碱式碳酸铜[Cu2(OH)2CO3]的质量分数.称取该铜矿样品30g于烧杯中,逐滴滴入132 2g稀盐酸至刚好完全反应,生成CO2气体4 4g(假设
小羽从试剂商店购得一瓶质量分数为30%的双氧水 配制120g5%的双氧水 全部用于制氧气 则双氧水完
小羽从试剂商店购得一瓶质量分数为30%的双氧水,配制120g5%的双氧水,全部用于制氧气,则双氧水完全分解生成氧气的质量约为[ ]A.3 2 gB.2 8 gC.2 4 gD.1 6 g
节约资源和保护环境已经成为我们的基本国策.节能减排 环境保护和生态市建设是市政府今后五年的重点工作.
节约资源和保护环境已经成为我们的基本国策.节能减排、环境保护和生态市建设是市政府今后五年的重点工作.环保部门对某工厂的废水进行抽样分析,结果表
将6.5g石灰石样品投入到36.5g稀盐酸溶液中制取二氧化碳气体 恰好完全反应。反应后将溶液过滤 干
将6 5g石灰石样品投入到36 5g稀盐酸溶液中制取二氧化碳气体,恰好完全反应。反应后将溶液过滤、干燥,称量剩余固体残渣的质量为1 5g(提示:①石灰石样品
氯化钠是一种重要的化工原料。电解氯化钠溶液可制得氯气 氢氧化钠等物质 反应的化学方程式为2NaCl+
氯化钠是一种重要的化工原料。电解氯化钠溶液可制得氯气、氢氧化钠等物质,反应的化学方程式为2NaCl+2H2OCl2↑+H2↑+2NaOH。现取一定质量的氯化钠溶液进












