氯化钠是一种重要的化工原料。电解氯化钠溶液可制得氯气 氢氧化钠等物质 反应的化学方程式为2NaCl+
氯化钠是一种重要的化工原料。电解氯化钠溶液可制得氯气、氢氧化钠等物质,反应的化学方程式为2NaCl+2H2O Cl2↑+H2↑+2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠恰好完全反应时,得到51.2g溶液,生成氯气的质量与时间的关系如下图所示。请计算: Cl2↑+H2↑+2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠恰好完全反应时,得到51.2g溶液,生成氯气的质量与时间的关系如下图所示。请计算: |
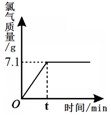 |
| (1)氯化钠完全反应时,溶液中剩余水的质量。 (2)原氯化钠溶液中溶质的质量分数。 (3)若把这些氯化钠溶液稀释成溶质的质量分数为0.9%的生理盐水,需要加水的质量。 |
参考解答
| 解:(1)设消耗氯化钠的质量为x,生成氢氧化钠的质量为y,生成氢气的质量为z 2NaCl+2H2O  Cl2↑+H2↑+2NaOH Cl2↑+H2↑+2NaOH2×58.5 71 2 2×40 x 7.1g z y 得方程(2×58.5):71=x:7.1g 71:(2×40)=7.1g:y 71:2=7.1g:z 解得x=11.7g;y=8g;z=0.2g ∴剩余水的质量:51.2g-8g=43.2g (2)氯化钠溶液质量为:51.2g+7.1g+0.2g=58.5g 氯化钠溶液中溶质的质量分数为: 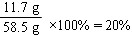 (3)设稀释后生理盐水的质量为a。58.5g×20%=a×0.9% a=1300g 需要加水的质量为:1300g-58.5g=1241.5g 答:(1)氯化钠完全反应时,溶液中剩余水的质量为43.2g。 (2)原氯化钠溶液中溶质的质量分数为20%。 (3)若把这些氯化钠溶液稀释成0.9%的生理盐水,需要加水的质量为1241.5g。 (其它合理解法同样给分) |
相似问题
某课外兴趣小组对实验室中的一瓶稀硫酸样品进行分析。他们分别用100g稀硫酸与不同质量的锌粒(含杂质
某课外兴趣小组对实验室中的一瓶稀硫酸样品进行分析。他们分别用100g稀硫酸与不同质量的锌粒(含杂质,杂质不与稀硫酸反应)反应,三次实验的数据如下表
将6.38克某纯净的铁的氧化物 与足量的一氧化碳在加热的条件下完全反应 反应生成的气体被足量石灰水完
将6 38克某纯净的铁的氧化物,与足量的一氧化碳在加热的条件下完全反应,反应生成的气体被足量石灰水完全吸收后,得到白色沉淀11克.试通过计算求此铁的
现有一含杂质的固体氯化钡样品(杂质不溶于水)。取12.5g样品放入烧杯中 然后加入39.6g水使其充
现有一含杂质的固体氯化钡样品(杂质不溶于水)。取12 5g样品放入烧杯中,然后加入39 6g水使其充分溶解,静置后滤去杂质。取10g滤液加入足量的硝酸银溶液
某研究小组为测定黄铜(铜锌合金)中锌的含量 用100g黄铜和足量的稀盐酸反应 结果得到了12g氢气。
某研究小组为测定黄铜(铜锌合金)中锌的含量,用100g黄铜和足量的稀盐酸反应,结果得到了12g氢气。请问该黄铜中锌的质量分数是多少?(列出计算过程)
某校化学实验室有一瓶标签残缺的过氧化氢溶液(如图所示)。该校化学课外兴趣小组的同学为了测定其中溶质的
某校化学实验室有一瓶标签残缺的过氧化氢溶液(如图所示)。该校化学课外兴趣小组的同学为了测定其中溶质的质量分数,他们取出该溶液34g,加入适量催化剂












